凋亡抑制蛋白(inhibitor of apoptosis proteins,IAPs)作为一种高度保守的程序性细胞死亡(凋亡)的内源性抑制剂[1],最初在杆状病毒中被发现[2-3],后来人们发现,IAPs广泛存在于病毒、细菌、酵母、昆虫和哺乳动物中,对细胞凋亡有较强的抑制作用[4]。IAPs是一个多功能蛋白家族,除行使抗凋亡功能外,在受体信号转导、细胞分裂、铜代谢和泛素化蛋白质等方面也发挥着重要作用[5-6]。IAPs家族蛋白结构的共同特点是氨基端含有数量不等的杆状病毒IAP重复序列(baculoviral IAP repeat,BIR),羧基端不包含或包含1个RING(really interesting new gene)指环结构。其中,BIR结构域负责介导蛋白质间的相互作用,使得一些IAPs能够直接结合并抑制半胱氨酸蛋白酶(Caspases)的催化活性,从而阻断细胞凋亡进程[7]。而IAPs羧基末端的RING指环结构域则提供了E3泛素连接酶活性,可以将下游靶蛋白泛素化,进而导致目标蛋白被降解[8-10]。
X染色体连锁凋亡抑制蛋白(X-linked inhibitor of apoptosis protein,XIAP)作为IAPs基因家族中重要的成员之一,该蛋白包含3个BIR结构域和1个RING指环结构域[11]。研究表明,XIAP的抗凋亡功能是通过BIRs与Caspase-3、Caspase-7和Caspase-9活性位点的直接相互作用实现的[12-13]。此外,有研究表明,XIAP除具有抑制Caspase的催化活性外,还在NF-κB和MAPKs等炎症信号通路中发挥作用[14-15]。有研究报道,相比于正常小鼠,XIAP缺陷小鼠在感染李斯特菌Listeria后其存活率显著降低, XIAP的存在促进了机体在感染李斯特菌时促炎症细胞因子的产生[16]。Damgaard等[17]研究发现,XIAP的BIR2结构域是X染色体连锁的淋巴细胞增生综合征2型(X-linked lymphoproliferative syndrome type-2, XLP2)错义突变的热点,并证明XLP2-BIR2突变严重损害了来自XLP2患者的原代细胞和重组的XIAP缺陷细胞系中NOD1/2依赖性的免疫信号。XIAP作为凋亡抑制蛋白家族中最受关注的成员,其生物学功能在很大程度上还是归因于其对细胞凋亡通路的抑制作用,然而,近年来的研究不断发现,其在调节炎症信号和免疫方面均发挥着重要作用[18]。截至目前,有关XIAP的相关报道大多局限于哺乳动物中,而在水产养殖动物中的研究非常缺乏。
虾夷马粪海胆Strongylocentrotus intermedius又称中间球海胆,原产于日本,1989年被引入中国,现已成为中国北方沿海地区重要的海胆养殖种类。本研究中,对虾夷马粪海胆XIAP基因进行了克隆,检测了XIAP基因在不同组织中的表达,同时检测了经不同免疫刺激物刺激后体腔细胞中XIAP基因的表达情况,以期为虾夷马粪海胆天然免疫系统的研究提供科学参考。
1 材料与方法
1.1 材料
试验用虾夷马粪海胆(2龄)取自大连海洋大学农业农村部北方海水增养殖重点实验室,体质量为40~80 g,海胆饲养于16~23 ℃海水中,每日投喂新鲜海带,取样前一日停止投喂。
1.2 方法
1.2.1 试验动物组织的获取 选取8枚健康虾夷马粪海胆(雌、雄各4枚),分别用注射器抽取体腔液,将收集到的体腔液在4 ℃下以5 000 r/min离心10 min,弃上清,收集体腔细胞,随后解剖虾夷马粪海胆,依次获取管足(tube foot)、围口膜(peristomial membrane)、肠(intestine)、精巢(testis)和卵巢(ovary)等组织,将组织块浸没于RNAlater(ThermoFisher)中,并在4 ℃冰箱中浸泡过夜,次日转移至-80 ℃超低温冰箱中保存,用于基因克隆和健康组织表达的实时定量分析。
在免疫刺激处理的过程中,选取强壮弧菌Vibrio fortis(革兰氏阴性菌)、葡聚糖(whole glucan particles, WGP)、肽聚糖(peptidoglycan, PGN)、脂多糖(lipopolysaccharide, LPS)和聚肌胞苷酸(polyinosinic-polycytidylic acid, Poly I:C)作为病原刺激物,以磷酸缓冲液(PBS)作为对照,分别对健康虾夷马粪海胆的体腔液进行活体注射。选择半致死剂量[19]的强壮弧菌进行注射,注射剂量为1.8×105 CFU/g,并注射50枚海胆,以防止海胆死亡导致试验样本数量不足;其余4种免疫刺激物每组各注射20枚,注射剂量为100 μL/枚,免疫刺激物浓度分别为脂多糖2 mg/mL、肽聚糖200 μg/mL、聚肌胞苷酸2 μg/mL、葡聚糖600 μg/mL;对照组20枚,用磷酸缓冲液注射,注射剂量为100 μL/枚。分别在注射后0、6、12、24、48、72 h抽取海胆体腔液(每个时间点各抽取3枚海胆体腔液),离心后弃上清液,收集体腔细胞浸没于RNAlater中,于4 ℃冰箱中过夜,次日转移至-80 ℃超低温冰箱中保存,用于组织基因表达的实时定量分析。
1.2.2 总RNA提取及cDNA第一链的合成 采用动物组织总RNA提取试剂盒(天根生化科技有限公司)对虾夷马粪海胆各组织总RNA及免疫刺激后体腔细胞的总RNA进行提取。采用核酸蛋白检测仪与10 g/L琼脂糖凝胶电泳检测总RNA浓度及完整性,将总RNA样品保存于-80 ℃超低温冰箱中备用。为减少个体差异及性别对试验结果的影响,精巢、卵巢各采用4枚雄性和4枚雌性海胆总RNA按浓度进行等量混合,其余各组织均采用6枚海胆(雌、雄各3枚)的总RNA按浓度进行等量混合,经5种免疫刺激物刺激后的6个时间点各提取3枚海胆的总RNA,然后将总RNA按浓度进行等量混合,将混合后的总RNA分别采用cDNA第一链合成试剂盒(北京全式金生物技术有限公司)合成cDNA第一链,得到的反转录产物于-80 ℃超低温冰箱中保存备用。
1.2.3 XIAP基因的cDNA克隆 基于从虾夷马粪海胆转录组数据[20]中筛选到的XIAP基因部分片段,应用Primer 5.0软件设计RACE引物XIAP-3、XIAP-5(表1),以体腔细胞总RNA合成的cDNA第一链为模板,采用SMARTer RACE cDNA Amplification Kit(Clontech公司)进行RACE克隆,分别用 XIAP-3和XIAP-5与试剂盒中的UPM引物配对进行PCR反应。反应体系(共25 μL):LA PCR buffer(10×)2.5 μL,cDNA 2 μL,dNTPs 2 μL,UPM 2 μL,XIAP-3 0.5 μL,XIAP-5 0.5 μL,LA Taq 0.25 μL,用ddH2O补足至25 μL。采用以下程序进行降落PCR反应:94 ℃下预变性5 min;94 ℃下变性30 s,72 ℃下退火与延伸3 min 30 s,共进行5个循环;94 ℃下变性30 s,70 ℃下退火复性30 s,72 ℃下延伸3 min,共进行5个循环;94 ℃下变性30 s,65 ℃下退火复性30 s,72 ℃下延伸3 min,共进行30个循环;最后在72 ℃下再延伸7 min,4 ℃下保存。用10 g/L琼脂糖凝胶电泳检测PCR产物质量。
表1 XIAP基因所用引物
Tab.1 Primers for XIAP Gene
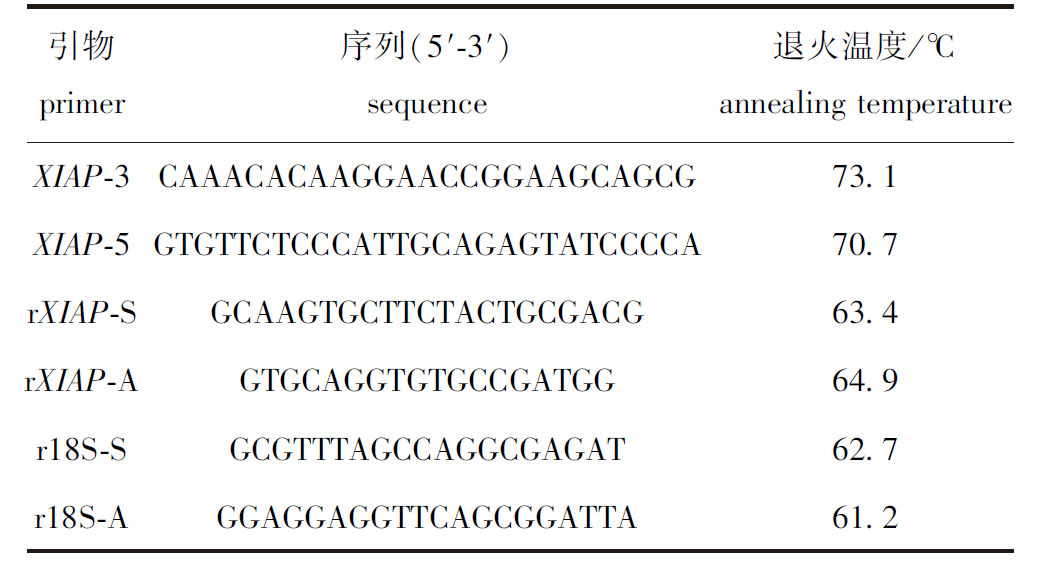
引物 primer序列(5'-3')sequence退火温度/℃ annealing temperatureXIAP-3CAAACACAAGGAACCGGAAGCAGCG73.1XIAP-5GTGTTCTCCCATTGCAGAGTATCCCCA70.7rXIAP-SGCAAGTGCTTCTACTGCGACG63.4rXIAP-AGTGCAGGTGTGCCGATGG64.9r18S-SGCGTTTAGCCAGGCGAGAT62.7r18S-AGGAGGAGGTTCAGCGGATTA61.2
采用凝胶回收试剂盒(北京全式金生物技术有限公司)回收目的条带,将回收的cDNA片段连接到pEASY-T1载体(北京全式金生物技术有限公司)上,将连接好的质粒转化到DH5α大肠杆菌感受态细胞(北京全式金生物技术有限公司)中,再将细菌培养液均匀涂布于含氨苄西林、IPTG、X-gal的LB固体培养基上培养(37 ℃)12~16 h,挑取白色单菌落小量培养,采用M13通用引物进行菌液PCR扩增,选取阳性克隆菌液送上海英骏生物技术有限公司测序。
1.2.4 生物信息学分析 采用NCBI在线工具BlastX(https://blast.ncbi.nlm.nih.gov/Blast.cgi)对拼接后的测序结果进行比对,得到的目标序列提交到NCBI的ORF Finder (https://www.ncbi.nlm. nih.gov/orffinder/)查找其开放阅读框;采用在线工具ExPASy (https://www.expasy.org/resources)预测XIAP蛋白的相对分子质量和等电点,并提交到NCBI的Protein BLAST (https://blast.ncbi. nlm.nih.gov/Blast.cgi),对所得氨基酸序列进行同源性分析;采用MEGA 7.0软件与其他物种的氨基酸序列相似性进行比对,并构建系统进化树;使用DNASTAR软件包中的MegAlign程序计算相似指数和分化指数,并采用SMART(http://smart.embl-heidelberg.de/)在线工具预测XIAP蛋白的保守结构域。
1.2.5 组织表达特征分析 分别以“1.2.2节”中6种健康组织和经5种免疫刺激物刺激体腔细胞后的6个不同时间点获得的cDNA第一链为模板,采用实时定量PCR检测XIAP基因在各健康组织,以及经免疫刺激后在体腔细胞中的相对表达量。内参基因选取18S rRNA,根据GenBank中虾夷马粪海胆的18S rRNA序列设计(Accession:D14365)正、反向引物r18S-S、r18S-A(表1)。反应体系(共20 μL):2× SYBR Realting PCR Master Mix 10 μL,正、反向引物rXIAP-S、rXIAP-A(表1)各0.8 μL,cDNA模板2 μL,RNase free H2O 6.4 μL。PCR扩增程序采用二步法:95 ℃下预变性30 s;95 ℃下变性5 s,60 ℃下退火34 s,共进行40个循环。每个样本均进行3次技术重复。
采用2-ΔΔCt法计算XIAP基因在虾夷马粪海胆6种健康组织中的表达量,以及经免疫刺激后XIAP基因在体腔细胞中的表达量。其中,经免疫刺激后XIAP基因在体腔细胞中的相对表达量是以注射PBS的对照组作为背景,数据表示为相对于基线水平(PBS 处理)的表达变化倍数。
1.3 数据处理
试验结果以平均值±标准误(mean±S.E.)表示,利用SPSS 19.0软件进行单因素方差分析,采用Duncan法进行组间多重比较,显著性水平设为0.05。
2 结果与分析
2.1 基因序列分析
将PCR、5′ RACE和3′ RACE获得的3个片段拼接后得到长度为4 894 bp的虾夷马粪海胆XIAP cDNA序列(图1)。该序列包括459 bp的5′非编码区(UTR)、2 331 bp开放阅读框(ORF)和2 104 bp的3′非编码区(UTR)。序列已提交到GenBank(登录号为OM209992)。虾夷马粪海胆XIAP基因的cDNA可编码776个氨基酸,用ExPASy预测该蛋白的相对分子质量为86 960,等电点为5.96,为酸性蛋白。将获得的XIAP基因ORF序列提交到NCBI数据库进行比对,发现虾夷马粪海胆XIAP氨基酸序列与紫海胆XIAP序列的同源性最高,一致性为91.6%(表2),确定该基因为虾夷马粪海胆X染色体连锁凋亡蛋白抑制因子(X-linked inhibitor of apoptosis, XIAP)基因。SMART结构域预测结果显示,虾夷马粪海胆XIAP蛋白具有3个BIR结构域(84 aa~155 aa,241 aa~312 aa,375 aa~448 aa)和1个RING指环结构域(729 aa~763 aa)(图1)。

*表示终止密码子;方框部分表示BIR结构域;阴影方框部分表示RING指环结构域。
Asterisk (*) indicates the stop codons;BIR domains are shown in blank box and the shadow box shows RING finger domain.
图1 虾夷马粪海胆XIAP基因cDNA序列及预测的氨基酸序列
Fig.1 Full-length cDNA sequence and predicted amino acid sequence of XIAP in sea urchin Strongylocentrotus intermedius
表2 不同物种间XIAP基因序列的距离
Tab.2 Pair distances of XIAP nucleotide sequences among different species

物种speciesS.intermediusD.rerioB.taurusM.musculusM.yessoensisA.japonicasS.kowalevskiiC.gigasS.purpuratusA.planciL.obliquidensG.gallusX.laevisH.sapiensS.intermedius***31.930.431.024.625.440.419.191.630.230.631.435.230.8D.rerio148.9***44.945.822.727.735.622.932.333.345.243.044.244.9B.taurus157.694.6***87.122.427.034.821.130.030.091.559.155.987.9M.musculus153.591.914.2***23.225.835.321.130.230.689.959.856.089.5M.yessoensis198.0216.0219.0211.0***22.024.410.525.826.322.022.822.822.4A.japonicas194.9175.7181.4190.8223.0***26.712.025.728.725.825.327.325.5S.kowalevskii109.8130.0133.8131.2200.0183.2***22.240.034.733.834.836.133.8C.gigas257.0214.0233.0232.0487.0414.0221.0***18.319.320.821.921.620.8S.purpuratus8.9146.1160.1158.4191.2192.3111.5270.0***30.230.032.034.730.4A.planci158.8140.9160.1155.9186.9168.3134.0254.0158.8***29.929.635.430.0L.obliquidens156.293.89.010.9223.0191.5138.5237.0159.9160.3***59.957.491.5G.gallus151.2100.958.456.9215.0195.6133.4224.0147.8162.456.7***54.758.5X.laevis131.796.865.465.1215.0179.0127.6228.0134.0130.662.168.2***55.1H.sapiens155.194.613.211.3219.0194.2138.5237.0157.6160.19.059.767.1***
注: 对角线上方表示相似指数, 对角线下方表示分化指数。
Note: Percent similarity is shown in upper triangle and percent divergence is shown in lower triangle.
2.2 同源性分析
用MEGA 7.0软件对包括虾夷马粪海胆在内的14个不同物种的XIAP氨基酸序列(表3)进行同源性分析,用邻位相接法构建系统进化树,Bootstrap值设为1 000。结果显示:进化树分为两个分支,所有脊椎动物均较好地聚集在一个分支中,而所有海洋无脊椎动物均远离脊椎动物单独聚为一支;虾夷马粪海胆XIAP和紫海胆XIAP单独聚为一小支(图2)。这表明,虾夷马粪海胆的XIAP与紫海胆XIAP的亲缘关系最近。
表3 系统发育分析所用XIAP氨基酸序列
Tab.3 XIAP amino acid sequences used for phylogenetic analysis
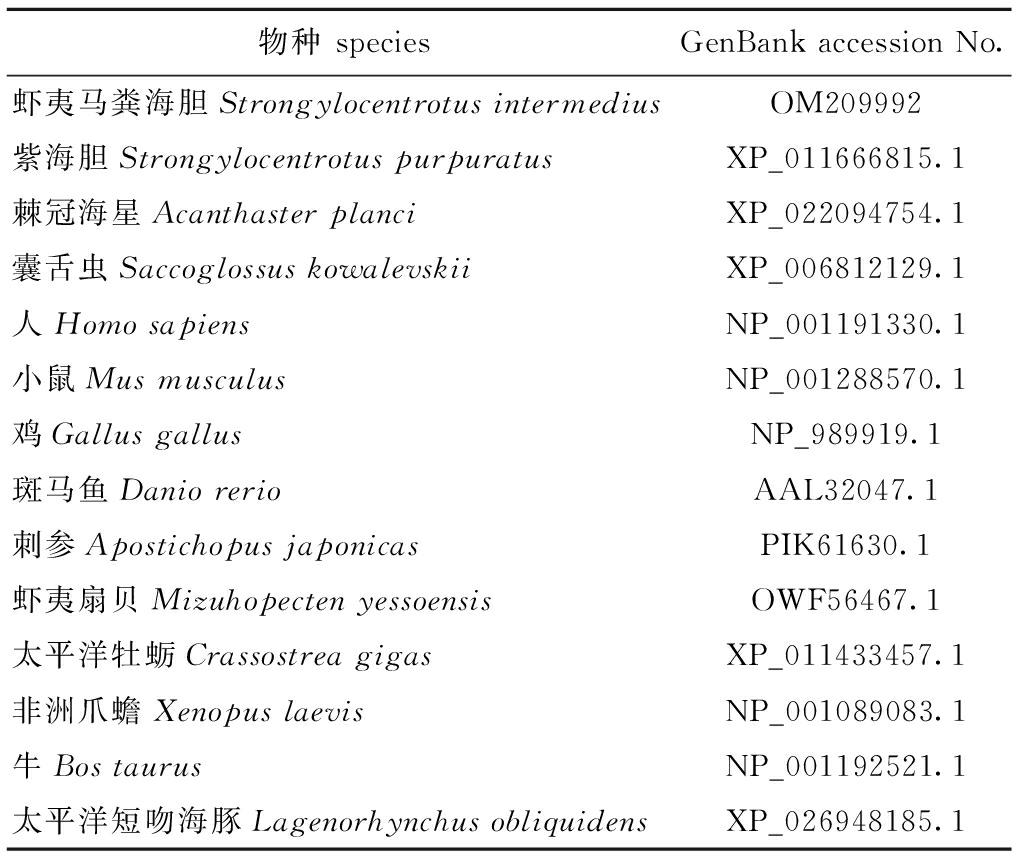
物种 speciesGenBank accession No.虾夷马粪海胆Strongylocentrotus intermediusOM209992紫海胆Strongylocentrotus purpuratusXP_011666815.1棘冠海星Acanthaster planciXP_022094754.1囊舌虫Saccoglossus kowalevskiiXP_006812129.1人Homo sapiensNP_001191330.1小鼠Mus musculusNP_001288570.1鸡Gallus gallusNP_989919.1斑马鱼Danio rerioAAL32047.1刺参Apostichopus japonicasPIK61630.1虾夷扇贝Mizuhopecten yessoensisOWF56467.1太平洋牡蛎Crassostrea gigasXP_011433457.1非洲爪蟾Xenopus laevisNP_001089083.1牛Bos taurusNP_001192521.1太平洋短吻海豚Lagenorhynchus obliquidensXP_026948185.1

图2 基于XIAP氨基酸序列构建的系统发育进化树
Fig.2 Phylogenetic tree based on XIAP amino acid sequences
2.3 XIAP蛋白结构域分析
利用SMART在线工具对包含虾夷马粪海胆、紫海胆和囊舌虫在内的11个物种的XIAP蛋白保守结构域进行预测(图3)。其中,脊椎动物(人、鸡、非洲爪蟾和斑马鱼)的XIAP蛋白包含3个BIR结构域和1个RING指环结构域,且第3个BIR结构域和RING指环结构域的距离相对较近;在虾夷马粪海胆、紫海胆、棘冠海星和囊舌虫的XIAP蛋白中同样含3个BIR结构域和1个RING指环结构域,除囊舌虫外,其余物种的第3个BIR结构域和RING指环结构域距离相对较远;刺参、太平洋牡蛎和虾夷扇贝XIAP蛋白的结构域不同于其他物种。从结构域的种类、数量及位置可知,脊椎动物的BIR结构域排布更加紧密,而虾夷马粪海胆与紫海胆的结构域在位置和种类上极为相似,符合系统发育进化树的分析结果。
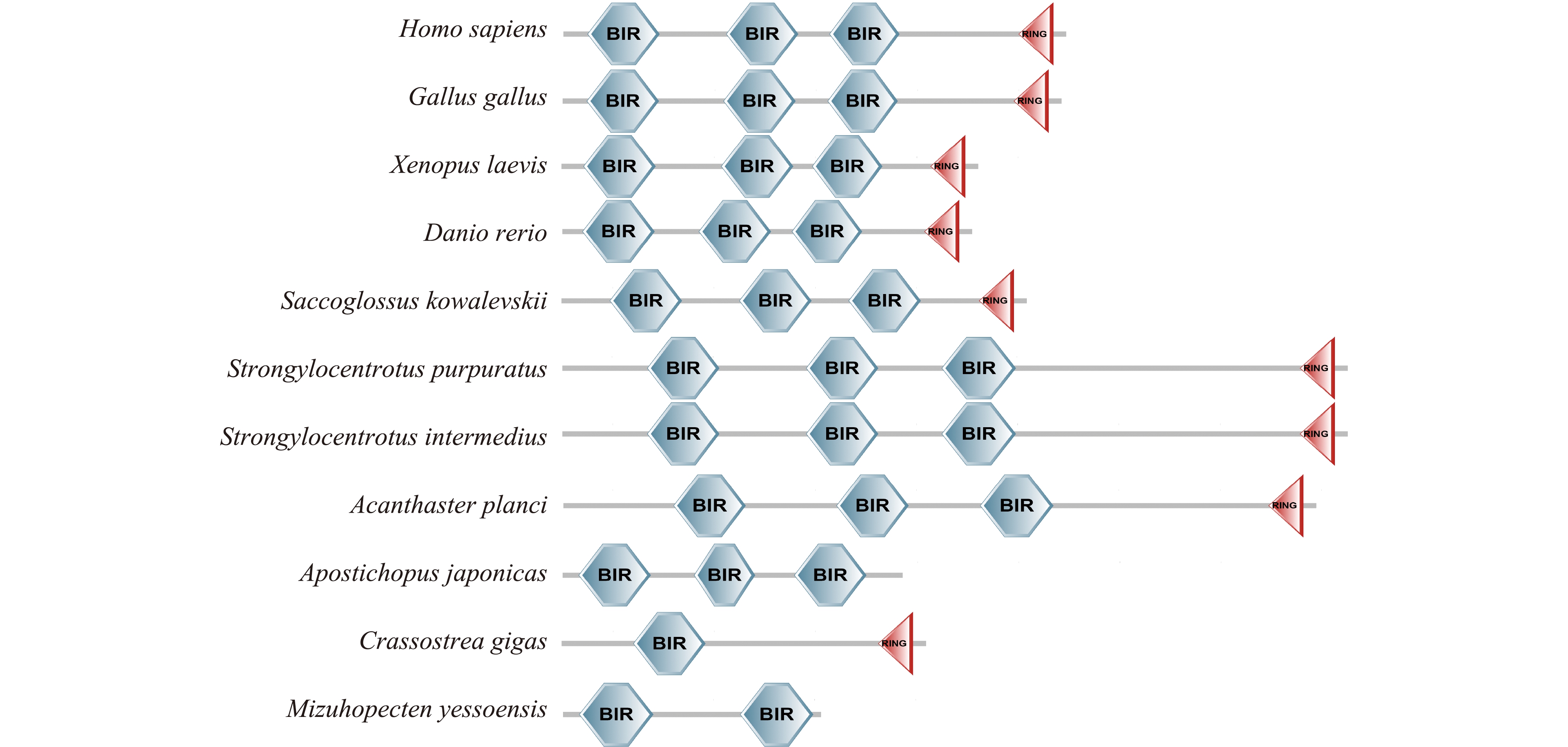
图3 基于XIAP氨基酸序列预测的蛋白结构域结果比较
Fig.3 Comparison of protein domain results based on XIAP amino acid sequence prediction
2.4 虾夷马粪海胆不同组织中XIAP基因的表达特征
采用实时定量PCR技术分析XIAP基因在虾夷马粪海胆选定组织中的相对表达情况。从图4可见,XIAP基因在虾夷马粪海胆所有被检测的组织中均有表达,但不同组织间的表达量有差异,XIAP基因在卵巢中表达量最高,且显著高于其他组织(P<0.05),在管足、围口膜、体腔细胞、肠和精巢5种组织中的表达量均较低,且无显著性差异(P>0.05)。
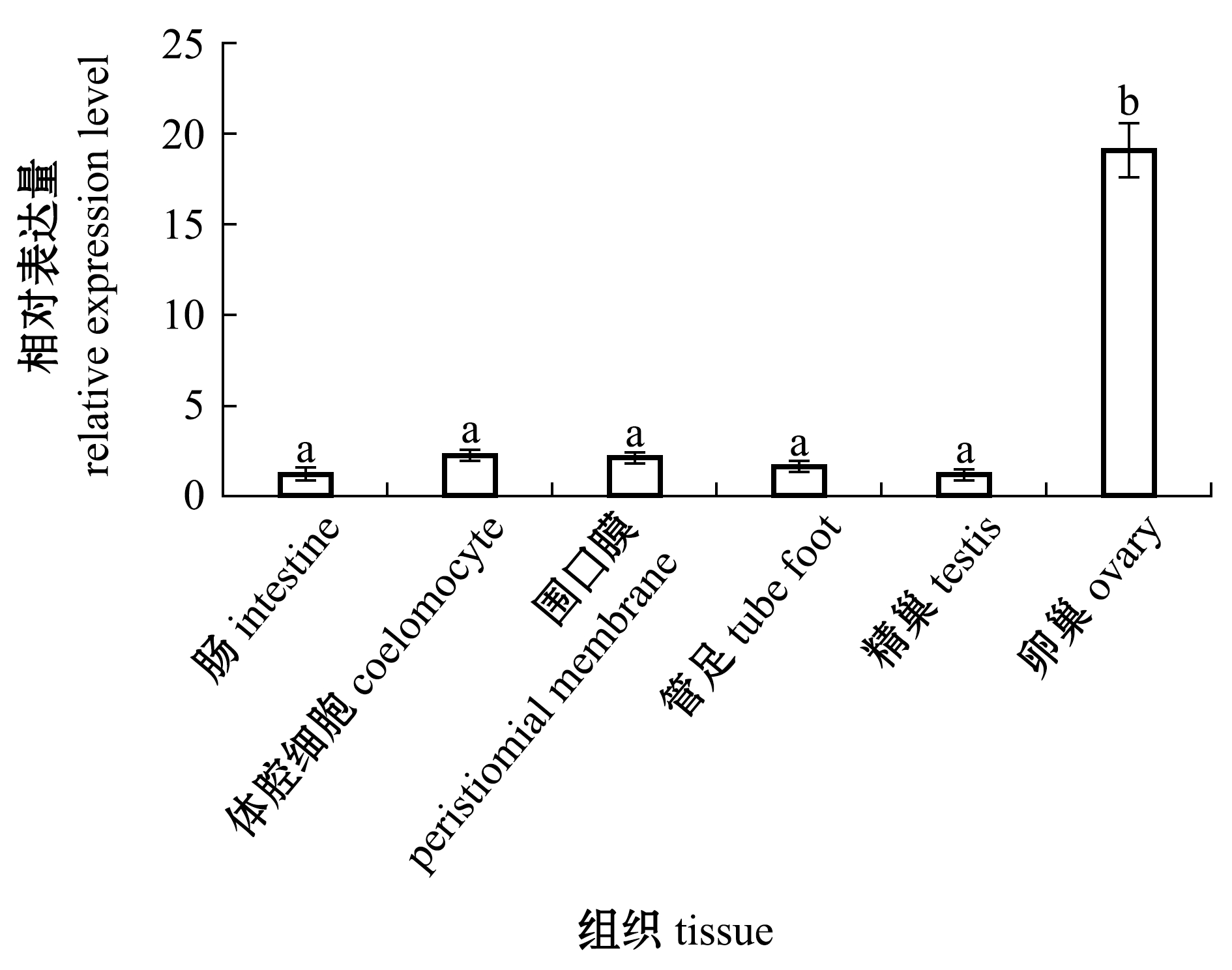
标有不同字母者表示组间有显著性差异(P<0.05),标有相同字母者表示组间无显著性差异(P>0.05)。
The means with different letters are significantly different in the groups at the 0.05 probability level, and the means with the same letter are not significant differences.
图4 虾夷马粪海胆不同组织中XIAP基因的表达
Fig.4 Expression level of XIAP gene in different tissues of sea urchin Strongylocentrotus intermedius
2.5 免疫刺激后体腔细胞中XIAP的表达特征
实时定量PCR结果显示,在5种免疫刺激物刺激虾夷马粪海胆体腔细胞后的6个时间点内,XIAP基因在体腔细胞中均有表达(图5)。经LPS刺激后, XIAP基因在0、6、24、48、72 h 5个时间点的表达量较低且无显著性差异(P>0.05),在12 h时表达量最高,且相较于0 h表达量显著性提高了11倍(P<0.05)。经PGN刺激后,0~12 h内XIAP基因表达量呈上升趋势,12 h时表达量最高,12 h后表达量开始下降,免疫刺激后的5个时间点的表达量全部高于0 h表达量,仅12、6 h时的表达量显著升高(P<0.05)。经Poly I:C刺激后,体腔细胞中XIAP基因表达量在12~24 h时呈显著性上升趋势(P<0.05),12 h时表达量最高,24 h时表达量略低于12 h,24~72 h时表达量逐渐下降至正常水平。经WGP刺激后,XIAP基因表达量分别在24 h和48 h时显著上调(P<0.05),其余4个时间点的表达量较低,且无显著性差异(P>0.05)。经V.fortis刺激后,体腔细胞中XIAP基因表达量在6 h时显著上调(P<0.05),12 h后降为正常水平。
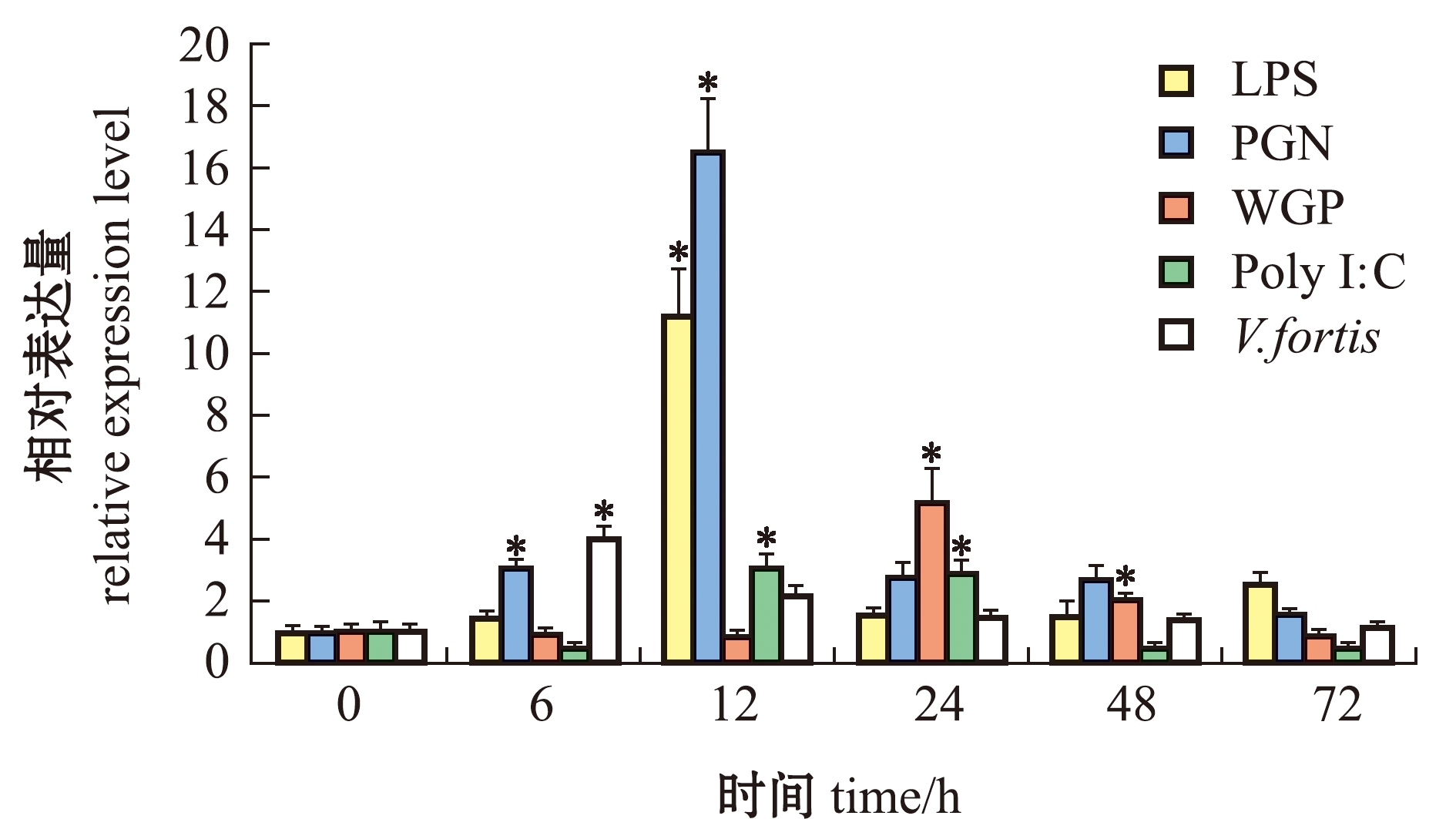
*表示同一种免疫刺激物刺激后XIAP基因在海胆体腔细胞中出现显著性差异表达的时间点(P<0.05)。
* indicates the time point at which the XIAP gene appears to be significantly differentially expressed in sea urchin coelomocytes after stimulation with the same immunostimulant (P<0.05).
图5 不同外源物刺激后XIAP基因在体腔细胞中的表达
Fig.5 Expression of XIAP gene in coelomocyte after stimulation with different exogenous agents
综上,5种免疫刺激物刺激虾夷马粪海胆体腔细胞后的6个时间点内,XIAP基因表达量在体腔细胞中总体呈现先升高后降低的趋势,但不同免疫物刺激后XIAP基因的上调程度不同,最高表达量也有较大差异。在WGP、Poly I:C和V.fortis刺激后,XIAP基因在体腔细胞中最高点的相对表达量在3.0~5.2范围内,而经PGN和LPS刺激后,XIAP基因在体腔细胞中最高点的相对表达量分别为16.5和11.25,且经PGN和LPS刺激后,XIAP的最高表达量相较于0 h时分别上调了16倍和11倍。
3 讨论
3.1 XIAP基因的功能分析
XIAP基因编码的蛋白一般含有3个BIR结构域和1个RING指环结构域[21]。本研究中,克隆获得的虾夷马粪海胆XIAP基因cDNA长为4 894 bp,开放阅读框共编码776个氨基酸,SMART蛋白结构域预测结果显示,XIAP包含3个BIR结构域和1个RING指环结构域,符合XIAP此类蛋白的结构特点。此外,不同物种XIAP蛋白的BIR结构域在进化上较为保守,该结构域由富含半胱氨酸/组氨酸(Cysteine/Histidine)的70个氨基酸序列组成[22]。
目前,研究者共发现8个IAPs成员: NAIP、 c IAP1、c IAP2、XIAP、Survivin、Apollon、 ML IAP和ILP 2。在人类IAP蛋白中,尽管其他IAP蛋白(NAIP、ML IAP、Survivin、ILP2和Apollon)也在细胞存活、细胞周期、炎症和整体稳态中发挥重要作用[23],但有关XIAP、c IAP1和c IAP2的研究相对较多。研究表明,XIAP在癌细胞中广泛表达且表达量显著增加。XIAP被确认的第一个功能是其抗凋亡活性。然而,与不是Caspases直接抑制剂的 c IAP1和c IAP2相比,XIAP 是一种有效的程序性细胞死亡抑制剂,因为它能够通过其BIR2和BIR3结构域直接阻断Caspases 3/7/9的活性[5]。除了其抗凋亡功能外,XIAP还被证明参与了多种信号通路[24-25]。XIAP的这些功能大多依赖于其促进蛋白质泛素化的能力,它能通过其RING结构域促进蛋白质泛素化,并能激活典型的NF-κB和MAPKs炎症信号通路。
3.2 XIAP基因参与的免疫信号通路分析
XIAP蛋白是IAPs蛋白家族中的一员,XIAP蛋白除抑制细胞凋亡外,还能够诱导NF-κB信号通路和MAP激酶(促分裂原活化蛋白激酶)的激活[26]。MAP激酶级联途径在内源、外源信号传导过程中发挥着重要作用,该途径可以调控细胞响应各种外源信号,使机体对各种环境胁迫做出响应。参与免疫反应的早期和炎症反应各阶段的许多分子也都受NF-κB的调控,另外一些抗炎及与细胞凋亡有关的分子也受NF-κB信号通路的调控,其中就包括抗细胞凋亡蛋白IAPs。本研究中,实时定量PCR结果显示,虾夷马粪海胆的6种健康组织中均检测到XIAP基因的转录本,其中,卵巢中的表达量最高,在精巢中也有表达,但表达量显著低于卵巢。本试验取样时正值海胆性腺成熟期,因此,笔者推测基因XIAP的高表达可能通过发挥免疫作用保护卵子免受病原体侵害。内毒素是革兰氏阴性细菌细胞壁的一个重要组成部分,通常在细菌裂解后释放,其主要化学成分是脂多糖,作为细菌入侵生物体时的主要抗原分子,脂多糖的信号主要通过TLR 4实现跨膜转导,并诱导机体发生免疫反应[27]。本研究中,脂多糖刺激海胆体腔细胞后,虾夷马粪海胆XIAP在12 h时出现表达上调,表明XIAP在免疫刺激后参与了海胆TLR信号通路的调控。肽聚糖是NLR信号通路中的一个主要模式识别受体,NLR信号通路中肽聚糖的识别可以通过细胞凋亡抑制剂激活RIP2,然后激活NF-κB信号通路[28]。本研究中,当海胆受到肽聚糖的刺激后,体腔细胞中XIAP表达量在12 h时显著性上调,推测是肽聚糖在免疫刺激后被海胆NLR信号通路识别,此时XIAP蛋白发挥了细胞凋亡抑制剂的作用,激活了NF-κB信号通路,使海胆对外界刺激做出免疫应答反应。聚肌胞苷酸是一种合成型双链RNA (dsRNA)的类似物,一种病毒感染相关的分子模式,可部分模拟病毒感染的免疫激活机制。本研究中,以聚肌胞苷酸刺激海胆体腔细胞来模拟RNA病毒在RLR信号通路中识别的配体,在配体被识别后介导CARD 9复合体组装,然后激活 NF-κB信号通路[29-30],经聚肌胞苷酸刺激后,体腔细胞中XIAP基因表达量在12~24 h时呈显著性上调,推测XIAP基因参与了海胆的RLR信号通路。葡聚糖是真菌细胞壁基质的主要成分,是CLR信号通路中的C型凝集素受体的配体[31],当葡聚糖作为配体被受体识别后,非受体酪氨酸蛋白激酶(protein tyrosine kinase, TPK)被激活,然后介导CARD9复合体组装,并激活NF-κB信号通路。本研究中,当用葡聚糖对虾夷马粪海胆的体腔细胞进行免疫刺激,XIAP基因表达量在刺激后的24 h时出现显著性上调趋势,这表明XIAP基因参与了海胆CLR信号通路的调控。强壮弧菌是虾夷马粪海胆的一种致病菌,本研究中,在海胆体腔细胞受到强壮弧菌刺激后的6 h时,XIAP基因表达量出现显著性上调,随后表达量开始下降,直到72 h时降至正常水平,这表明XIAP基因参与了虾夷马粪海胆的免疫应答,在海胆的免疫中发挥了作用。
NF-κB信号通路是重要的转录调控因子,调控细胞的多种基因表达,与细胞的增殖、免疫应答、炎症反应有关。IAPs能够通过调控NLR、TLR、RLR和CLR信号通路进而激活NF-κB信号通路,因此,在几乎所有病原体刺激海胆体腔细胞时,XIAP基因表达量均出现上调的趋势,说明XIAP在4种信号通路的上游信号向下游传递过程中可能起到至关重要的作用,且XIAP作为凋亡抑制因子可以保护细胞在病原入侵时不被降解[32],因此,体腔细胞在经多种病原菌处理后XIAP基因的表达量均有不同程度的变化。本研究中,克隆获得了虾夷马粪海胆XIAP基因序列,并分析了其在不同外源物刺激后的表达量变化。结果显示,该基因参与了NLR、TLR、RLR和CLR 4种信号通路,相较于RLR和CLR信号通路,XIAP基因对NLR和TLR信号通路的调控更强,因此推测,XIAP可能在NLR和TLR信号通路中发挥了更加重要的调节功能。
4 结论
1)同源性及遗传进化树分析发现,虾夷马粪海胆的XIAP氨基酸序列与紫海胆XIAP氨基酸序列的同源性最高,与太平洋牡蛎氨基酸序列的同源性最低,符合物种进化规律。这表明,XIAP基因在海胆中具有一定的遗传保守性。
2) 实时定量PCR结果显示,XIAP基因在虾夷马粪海胆的6种健康组织中均有不同程度的表达,其中,在卵巢中的表达量最高,且与其他5种组织的表达量之间存在显著性差异。本试验取样时正值海胆性腺成熟期,笔者推测,基因XIAP在卵巢中的高表达,可能是为了通过发挥免疫作用来保护卵子免受病原体侵害。
3) 5种免疫刺激物刺激虾夷马粪海胆体腔细胞后的6个时间点内,XIAP基因在体腔细胞中的表达量总体呈现先升高后降低的趋势,但不同免疫物刺激后XIAP基因上调程度不同,最高表达量也有较大差异。这表明,XIAP基因在不同免疫物刺激后的不同时间点可能存在不同的调控作用,证实XIAP基因参与了虾夷马粪海胆的免疫应答,并在海胆的天然免疫中发挥重要作用。
[1] SALVESEN G S,DUCKETT C S.IAP proteins:blocking the road to death’s door[J].Nature Reviews Molecular Cell Biology,2002,3(6):401-410.
[2] CROOK N E,CLEM R J,MILLER L K.An apoptosis-inhibiting baculovirus gene with a zinc finger-like motif[J].Journal of Virology,1993,67(4):2168-2174.
[3] DUCKETT C S,NAVA V E,GEDRICH R W,et al.A conserved family of cellular genes related to the baculovirus iap gene and encoding apoptosis inhibitors[J].The EMBO Journal,1996,15(11):2685-2694.
[4] 许杨,赵晓航.IAP家族分子与肿瘤靶向治疗[J].生命科学,2010,22(2):161-168.
XU Y,ZHAO X H.IAP family and IAP-targeted cancer therapy[J].Chinese Bulletin of Life Sciences,2010,22(2):161-168.(in Chinese)
[5] ECKELMAN B P,SALVESEN G S,SCOTT F L.Human inhibitor of apoptosis proteins:why XIAP is the black sheep of the family[J].EMBO Reports,2006,7(10):988-994.
[6] MUFTI A R,BURSTEIN E,CSOMOS R A,et al.XIAP is a copper binding protein deregulated in Wilsons disease and other copper toxicosis disorders[J].Molecular Cell,2006,21(6):775-785.
[7] SRINIVASULA S M,ASHWELL J D.IAPs:what’s in a name?[J].Molecular Cell,2008,30(2):123-135.
[8] LI X M,YANG Y L,ASHWELL J D.TNF-RII and c-IAP1 mediate ubiquitination and degradation of TRAF2[J].Nature,2002,416(6878):345-347.
[9] WILSON R,GOYAL L,DITZEL M,et al.The DIAP 1 RING finger mediates ubiquitination of Dronc and is indispensable for regulating apoptosis[J].Nature Cell Biology,2002,4(6):445-450.
[10] HU S M,YANG X L.Cellular inhibitor of apoptosis 1 and 2 are ubiquitin ligases for the apoptosis inducer smac/DIABLO[J].The Journal of Biological Chemistry,2003,278(12):10055-10060.
[11] VAUX D L,SILKE J.IAPs,RINGs and ubiquitylation[J].Nature Reviews Molecular Cell Biology,2005,6(4):287-297.
[12] DEVERAUX Q L,TAKAHASHI R,SALVESEN G S,et al.X-linked IAP is a direct inhibitor of cell-death proteases[J].Nature,1997,388(6639):300-304.
[13] ROY N,DEVERAUX Q L,TAKAHASHI R,et al.The c-IAP-1 and c-IAP-2 proteins are direct inhibitors of specific caspases[J].The EMBO Journal,1997,16(23):6914-6925.
[14] BIRKEY REFFEY S,WURTHNER J U,PARKS W T,et al.X-linked inhibitor of apoptosis protein functions as a cofactor in transforming growth factor-beta signaling[J].The Journal of Biological Chemistry,2001,276(28):26542-26549.
[15] YAMAGUCHI K,SHIRAKABE K,SHIBUYA H,et al.Identification of a member of the MAPKKK family as a potential mediator of TGF-beta signal transduction[J].Science,1995,270(5244):2008-2011.
[16] BAULER L D,DUCKETT C S,O’RIORDAN M X D.XIAP regulates cytosol-specific innate immunity to Listeria infection[J].PLoS Pathogens,2008,4(8):e1000142.
[17] DAMGAARD R B,FIIL B K,SPECKMANN C,et al.Disease-causing mutations in the XIAP BIR 2 domain impair NOD 2-dependent immune signalling[J].EMBO Molecular Medicine,2013,5(8):1278-1295.
[18] JOST P J,VUCIC D.Regulation of cell death and immunity by XIAP[J].Cold Spring Harbor Perspectives in Biology,2020,12(8):a036426.
[19] WANG Y N,FENG N S,LI Q,et al.Isolation and characterization of bacteria associated with a syndrome disease of sea urchin Strongylocentrotus intermedius in North China[J].Aquaculture Research,2013,44(5):691-700.
[20] CHEN Y D,CHANG Y Q,WANG X L,et al.De novo assembly and analysis of tissue-specific transcriptomes revealed the tissue-specific genes and profile of immunity from Strongylocentrotus intermedius[J].Fish & Shellfish Immunology,2015,46(2):723-736.
[21] HOLCIK M,GIBSON H,KORNELUK R G.XIAP:apoptotic brake and promising therapeutic target[J].Apoptosis,2001,6(4):253-261.
[22] VERDECIA M A,HUANG H,DUTIL E,et al.Structure of the human anti-apoptotic protein survivin reveals a dimeric arrangement[J].Nature Structural Biology,2000,7(7):602-608.
[23] FULDA S,VUCIC D.Targeting IAP proteins for therapeutic intervention in cancer[J].Nature Reviews Drug Discovery,2012,11(2):109-124.
[24] GALB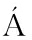 N S,DUCKETT C S.XIAP as a ubiquitin ligase in cellular signaling[J].Cell Death and Differentiation,2010,17(1):54-60.
N S,DUCKETT C S.XIAP as a ubiquitin ligase in cellular signaling[J].Cell Death and Differentiation,2010,17(1):54-60.
[25] KENNETH N S,DUCKETT C S.IAP proteins:regulators of cell migration and development[J].Current Opinion in Cell Biology,2012,24(6):871-875.
[26] LU M,LIN S C,HUANG Y H,et al.XIAP induces NF-kappaB activation via the BIR1/TAB1 interaction and BIR1 dimerization[J].Molecular Cell,2007,26(5):689-702.
[27] DUMITRU C D,CECI J D,TSATSANIS C,et al.TNF-alpha induction by LPS is regulated posttranscriptionally via a Tpl2/ERK-dependent pathway[J].Cell,2000,103(7):1071-1083.
[28] KOBAYASHI K,INOHARA N,HERNANDEZ L D,et al.RICK/Rip2/CARDIAK mediates signalling for receptors of the innate and adaptive immune systems[J].Nature,2002,416(6877):194-199.
[29] TAL M C,SASAI M W,LEE H K,et al.Absence of autophagy results in reactive oxygen species-dependent amplification of RLR signaling[J].Proceedings of the National Academy of Sciences of the United States of America,2009,106(8):2770-2775.
[30] EISEN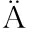 CHER K,KRUG A.Regulation of RLR-mediated innate immune signaling:it is all about keeping the balance[J].European Journal of Cell Biology,2012,91(1):36-47.
CHER K,KRUG A.Regulation of RLR-mediated innate immune signaling:it is all about keeping the balance[J].European Journal of Cell Biology,2012,91(1):36-47.
[31] DRUMMOND R A,SAIJO S,IWAKURA Y,et al.The role of Syk/CARD9 coupled C-type lectins in antifungal immunity[J].European Journal of Immunology,2011,41(2):276-281.
[32] COSSU F,MASTRANGELO E,MILANI M,et al.Designing smac-mimetics as antagonists of XIAP,cIAP1,and cIAP2[J].Biochemical and Biophysical Research Communications,2009,378(2):162-167.