智能响应型凝胶是能够在外界环境因素如温度、机械应力、光强度、pH、磁场和电场等刺激下,使其自身物理和化学变化性质发生突变的三维网络结构的亲水性聚合物[1-7]。由于此类凝胶可在不同环境下做出刺激响应,故可广泛应用于药物负载、靶向释药、组织修复和再生医学等领域[8-11]。其中,改变温度较其他因素相比容易控制且易于操作、成本又低[12],因此,智能凝胶中的温度响应型凝胶受到了广泛关注[13-14]。
聚氮烷基丙烯酰胺类温度响应型聚合物是制备温度响应型凝胶最常见的一种合成型高分子。由这类聚合物制备的温度响应型凝胶,能根据温度的变化实现其物理化学性质的改变,当凝胶处于室温时,凝胶呈现溶胀状态,当温度升高至体积相变温度(volume phase transition temperature,VPTT)时,凝胶脱水收缩,体积变小;随着温度恢复到室温时,凝胶再次吸水溶胀,恢复到初始形貌[15]。此类温度响应型凝胶在蛋白质传输系统、生物分离和医疗诊断等方面有着潜在应用[16-18]。为提高凝胶的生物相容性并扩大其应用范围,相关研究者将合成型温度响应高分子接枝到多糖分子骨架上,而后通过交联反应制备温度响应型凝胶;另一种制备多糖凝胶的方法是通过交联剂将合成温度响应高分子与多糖分子相连接制备块状多糖基复合凝胶。后者可有效避免有毒单体及引发剂等有毒物质的残留问题,因此,许多新型的智能凝胶都是通过该方法制备[19]。
海藻酸钠(sodium alginate,SA)是一种由α-L-古洛糖醛酸和β-D-甘露糖醛酸分子依据1→4键连接而成的天然多糖[20]。由于海藻酸钠优异的生物相容性、无毒性和生物降解性[21-22],其在食品工业、细胞培养和伤口愈合领域得到了广泛应用[23-25]。海藻酸钠分子骨架具有羧基和羟基等活性基团,这些基团不仅为交联反应的进行提供了活性位点,而且可以作为功能型官能团以实现凝胶的智能应用。本课题组前期制备了一系列具有温度响应性能的淀粉醚,此类淀粉醚产品为多支链结构,若与多糖复合制备凝胶材料,可制备多孔结构的温度响应型凝胶。另外,多糖/多糖型复合凝胶的主体均是由多糖组成,其生物降解性和生物相容性相比于合成型高分子/多糖型复合凝胶得到了极大的提升。
本研究中,以具有结构和性能优势的海藻酸钠和温度响应型淀粉(2-hydroxy-3-isopropoxypropyl starch,HIPS)为原料,以乙二醇二缩水甘油醚(ethylene glycol diglycidyl ether,EDGE)和氯化钙(CaCl2)为交联剂,利用共价键及离子键双重交联方法制备温度响应型淀粉/海藻酸钠(HIPS/SA)复合凝胶,优化其制备条件,并通过傅里叶转换红外光谱(FT-IR)、扫描电镜(SEM)表征凝胶的结构及微观形貌,同时研究了HIPS/SA复合凝胶的温度响应性能,以期为功能材料在药物缓释和分离工程等领域的应用提供新的途径。
1 材料与方法
1.1 材料
试剂:蜡质玉米淀粉购自国民淀粉化学股份有限公司(美国);海藻酸钠购自上海阿拉丁生化科技股份有限公司;无水氯化钙购自天津市科密欧化学试剂有限公司;乙二醇二缩水甘油醚购自东京化成工业株式会社。
仪器设备:SCIENTZ-10N超声波清洗机(SB-120T,宁波新芝生物科技股份有限公司);场发射高分辨率扫描电子显微镜(SU8010,株式会社日立制作所);在线红外光谱仪(Nicolet iS50,赛默飞世尔科技公司)。
1.2 方法
1.2.1 HIPS/SA复合凝胶的制备 将HIPS[异丙基缩水甘油醚(IPGE)与葡萄糖单元环(AGU)的摩尔比为2.5∶1]和海藻酸钠溶解于去离子水中,分别制得质量分数为6.5%的淀粉溶液和质量分数为4.0%的海藻酸钠溶液。在25 mL烧杯中混合2 g HIPS溶液和2 g 海藻酸钠溶液,加入300 μL 质量分数为40%的NaOH溶液并搅拌均匀,将混合物在冰水中超声振荡处理30 min。然后将270 μL EDGE和900 μL质量分数为1%的CaCl2加入上述混合溶液中,搅拌均匀,在冰水里超声振荡30 min,将烧杯转移至60 ℃的水浴中反应3 h。反应结束后,去掉烧杯中的水再加入去离子水并溶胀一段时间,随后将其在高温下加热,等待凝胶收缩,溶液变浑浊。再一次去掉烧杯中的水并重新加入去离子水溶胀,重复上述步骤,直至水溶液呈透明状态,这一现象表明,凝胶中未反应的小分子已基本去除。再将凝胶置于去离子水中溶胀2~3 d,在此期间反复换水,以保证达到完全去除未反应物质的目的。
1.2.2 不同反应条件对HIPS/SA复合凝胶溶胀率的影响
1)单因素反应条件优化试验。通过预试验得到每个因素的较佳反应条件后,微调反应条件进行单因素反应条件优化试验。制备HIPS/SA凝胶的反应中,设置HIPS质量分数为6.5%,海藻酸钠质量分数为4.0%,NaOH用量为300 μL,EDGE用量为300 μL,反应温度为55 ℃,反应时间为3 h。以溶胀率为指标,改变其中的一个因素,其他反应条件不变,研究该因素对HIPS/SA凝胶溶胀率的影响。HIPS质量分数分别设为5.0%、5.5%、6.0%、6.5%、7.0%;海藻酸钠质量分数分别设为3.0%、3.5%、4.0%、4.5%、5.0%;NaOH用量分别设为240、270、300、330、360 μL;EDGE用量分别设为240、270、300、330、360 μL;反应温度分别设为45、50、55、60、65 ℃;反应时间分别设为2.0、2.5、3.0、3.5、4.0 h。
2)反应条件组合优化的正交试验。为了优化反应条件,在正交试验设计中扩大数据采集的范围,每个因素各取5个水平,通过L25(56)正交试验确定HIPS/SA凝胶制备的最佳反应条件组合。
1.2.3 HIPS/SA凝胶形貌、结构及温度性能的表征
1)HIPS/SA凝胶形貌和结构表征。将20 ℃时达到吸水平衡的凝胶置入冰柜中冷冻12 h;将50 ℃时体积收缩的凝胶使用液氮快速冷冻,以保证冷冻后的凝胶结构不被破坏,随后用冷冻干燥机将凝胶冷冻干燥。从不同温度下保存的凝胶上取出部分凝胶样品,在样品表面进行喷金处理,通过扫描电镜表征其形貌(加速电压为10 kV),通过傅里叶转换红外光谱表征其结构。
2)HIPS/SA凝胶温度响应性能表征。采用质量法研究HIPS/SA凝胶的溶胀行为,将0.15 g的干燥凝胶置于0~50 ℃的去离子水中,加热速率为2.5 ℃/h,以保证凝胶达到溶胀平衡。将平衡溶胀率曲线斜率变化显著点的温度视为VPTT。凝胶的平衡溶胀率(RES)计算公式为
RES=(Ws-Wd)/Wd。
(1)
其中:Ws为在某一温度下达到溶胀平衡的凝胶质量(g);Wd为干燥凝胶质量(g)。
凝胶在给定温度下达到溶胀平衡后,用湿滤纸擦去凝胶表面的水分并称取凝胶质量。凝胶的溶胀率(RS)计算公式为
RS=(Wt-Wd)/Wd。
(2)
其中:Wt为凝胶在t(min)时刻的质量(g);Wd为干燥凝胶的质量(g)。
2 结果与分析
2.1 HIPS/SA凝胶的制备
在碱性条件下,将EDGE和CaCl2溶液与交联剂混合制备HIPS/SA凝胶的反应流程如图1所示,其过程是HIPS通过EDGE化学交联形成网络结构,海藻酸钠通过CaCl2溶液离子交联形成网络结构,两种网络结构互相贯穿形成互穿网络结构,最终制备成HIPS/SA凝胶。
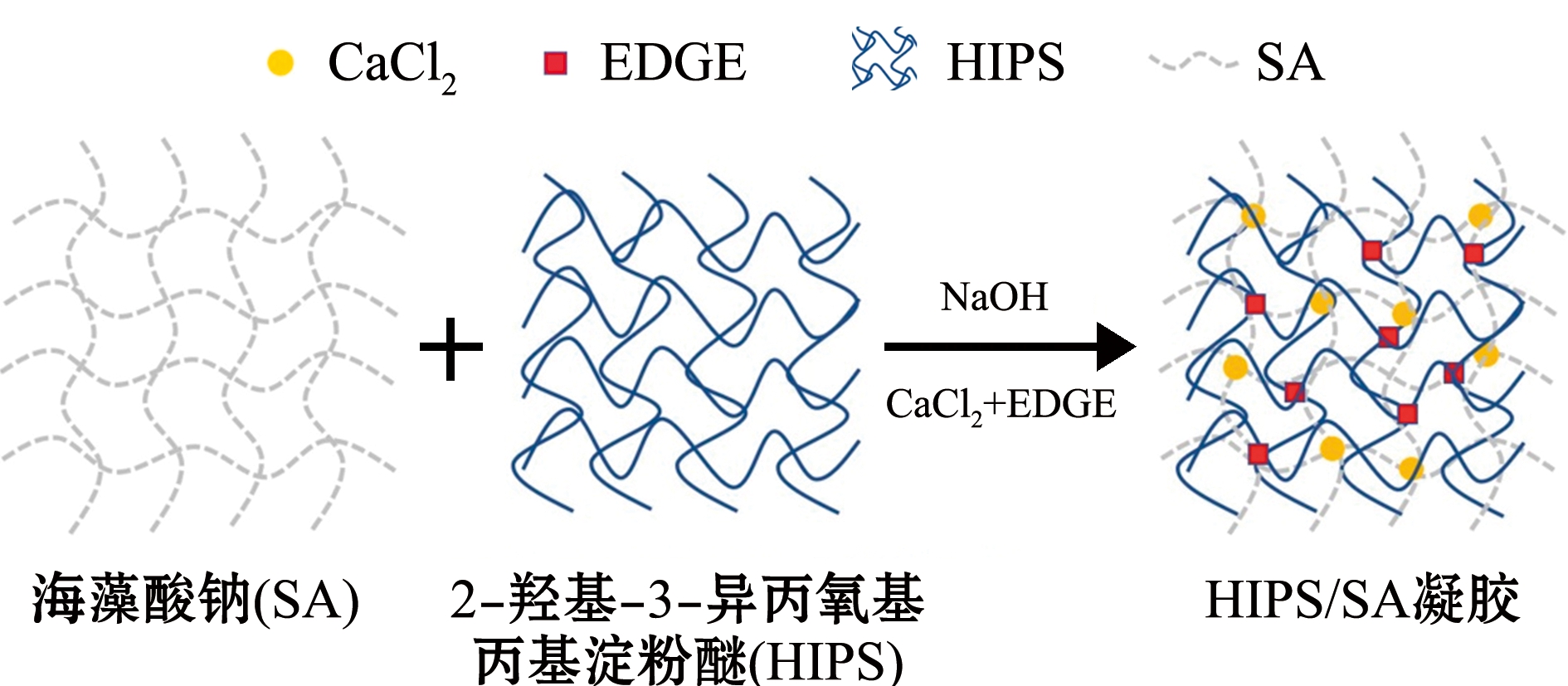
图1 HIPS/SA凝胶的反应过程
Fig.1 Process to prepare HIPS/SA composite hydrogel
2.2 HIPS/SA凝胶的结构表征
图2为SA、HIPS和HIPS/SA凝胶的傅里叶转换红外光谱。SA红外光谱中,1 594 cm-1附近是 —COO-中的C![]() O吸收峰,3 366 cm-1附近是O—H拉伸振动;HIPS红外光谱中,3 366、2 927、1 371、1 016 cm-1附近分别是O—H拉伸振动、C—H弯曲振动、CH2摇摆振动和C—O—C不对称拉伸吸收峰;而在HIPS/SA凝胶红外光谱中,1 628、1 371 cm-1附近分别是C
O吸收峰,3 366 cm-1附近是O—H拉伸振动;HIPS红外光谱中,3 366、2 927、1 371、1 016 cm-1附近分别是O—H拉伸振动、C—H弯曲振动、CH2摇摆振动和C—O—C不对称拉伸吸收峰;而在HIPS/SA凝胶红外光谱中,1 628、1 371 cm-1附近分别是C![]() O拉伸振动和CH2摇摆振动吸收峰。这表明,HIPS/SA凝胶中包含有SA和HIPS相应的结构特征峰,HIPS和SA分子链成功构成互穿网络结构,即HIPS/SA凝胶成功合成。
O拉伸振动和CH2摇摆振动吸收峰。这表明,HIPS/SA凝胶中包含有SA和HIPS相应的结构特征峰,HIPS和SA分子链成功构成互穿网络结构,即HIPS/SA凝胶成功合成。
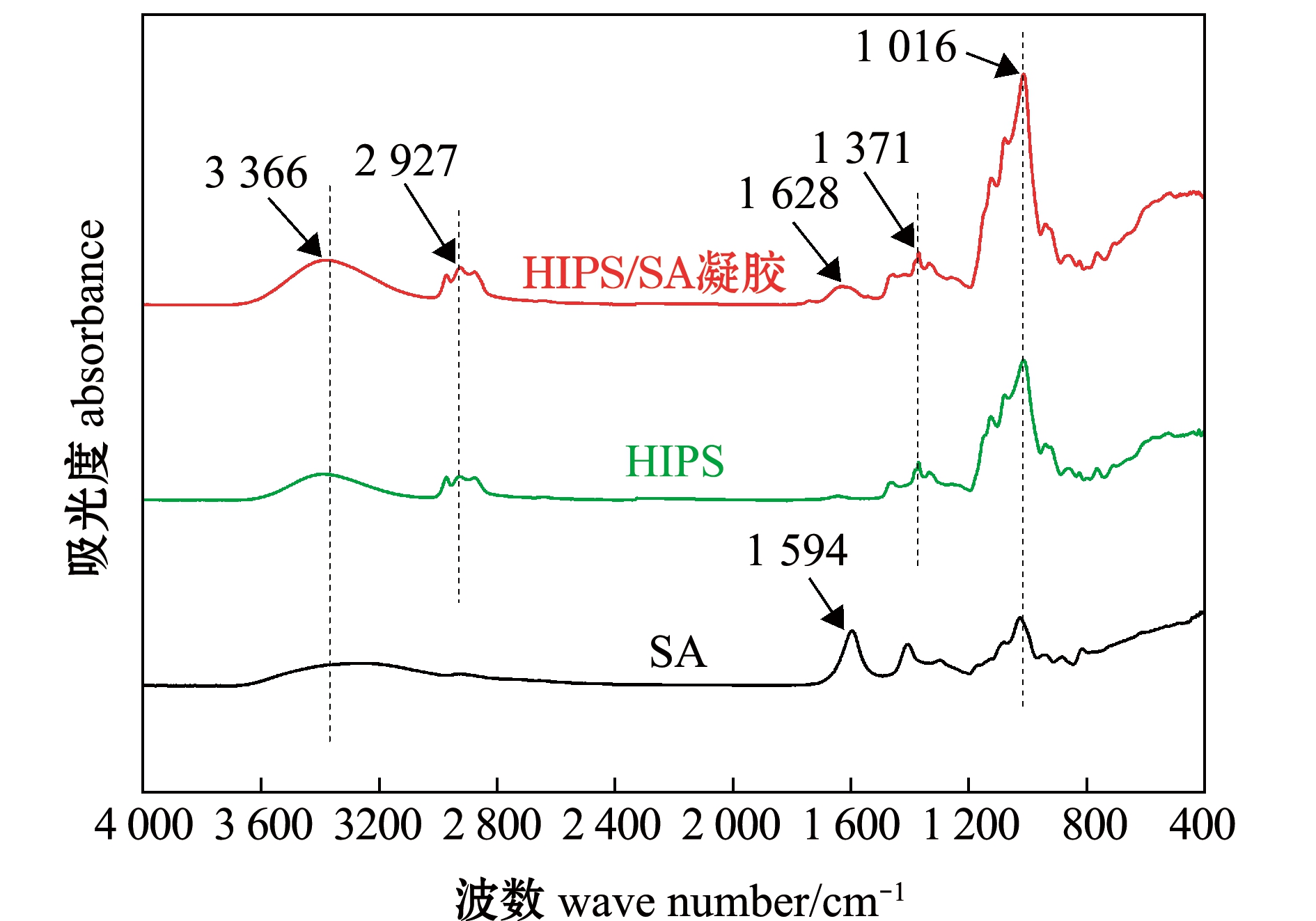
图2 SA、HIPS和HIPS/SA凝胶的红外光谱
Fig.2 FT-IR spectra of SA,HIPS and HIPS/SA hydrogel
2.3 不同反应条件对HIPS/SA凝胶溶胀率的影响
2.3.1 HIPS质量分数对HIPS/SA凝胶溶胀率的影响 从图3(a)可知,随着HIPS质量分数的增加,HIPS/SA凝胶的溶胀率呈不断上升趋势,并在HIPS质量分数达到6.5%时,HIPS/SA凝胶的溶胀率达到最大值(43.45),之后,随着HIPS质量分数的继续增加,凝胶的溶胀率开始逐渐下降。这是因为在HIPS质量分数达到6.5%前,随着HIPS质量分数的增加,交联反应的羟基数目越多,越易于形成交联网络,形成利于吸水的孔结构。但随着HIPS质量分数的进一步增加,交联密度过大,凝胶的吸水能力降低,最终导致凝胶的溶胀率下降。因此,本试验条件下,制备HIPS/SA凝胶的最佳HIPS质量分数为6.5%。
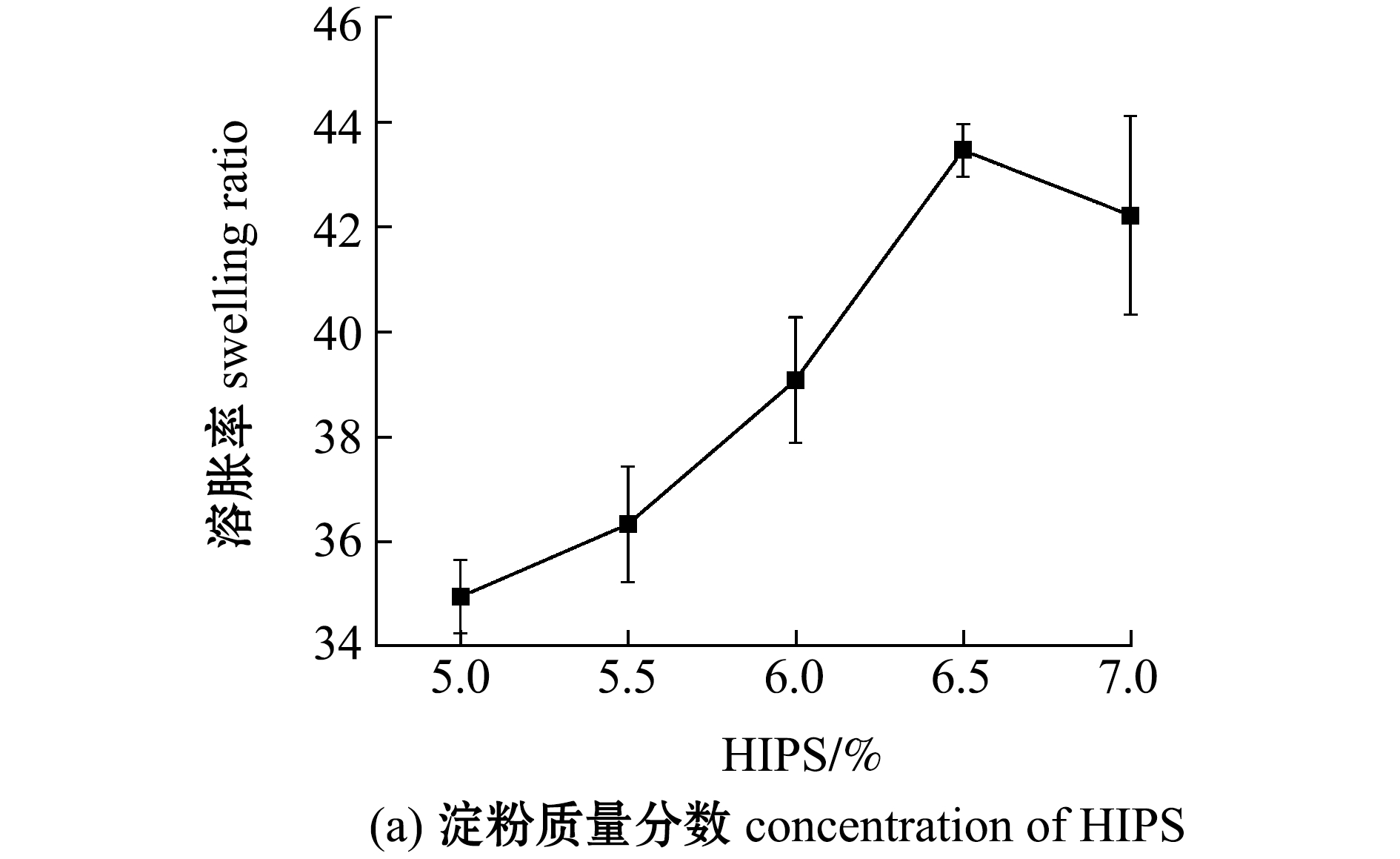
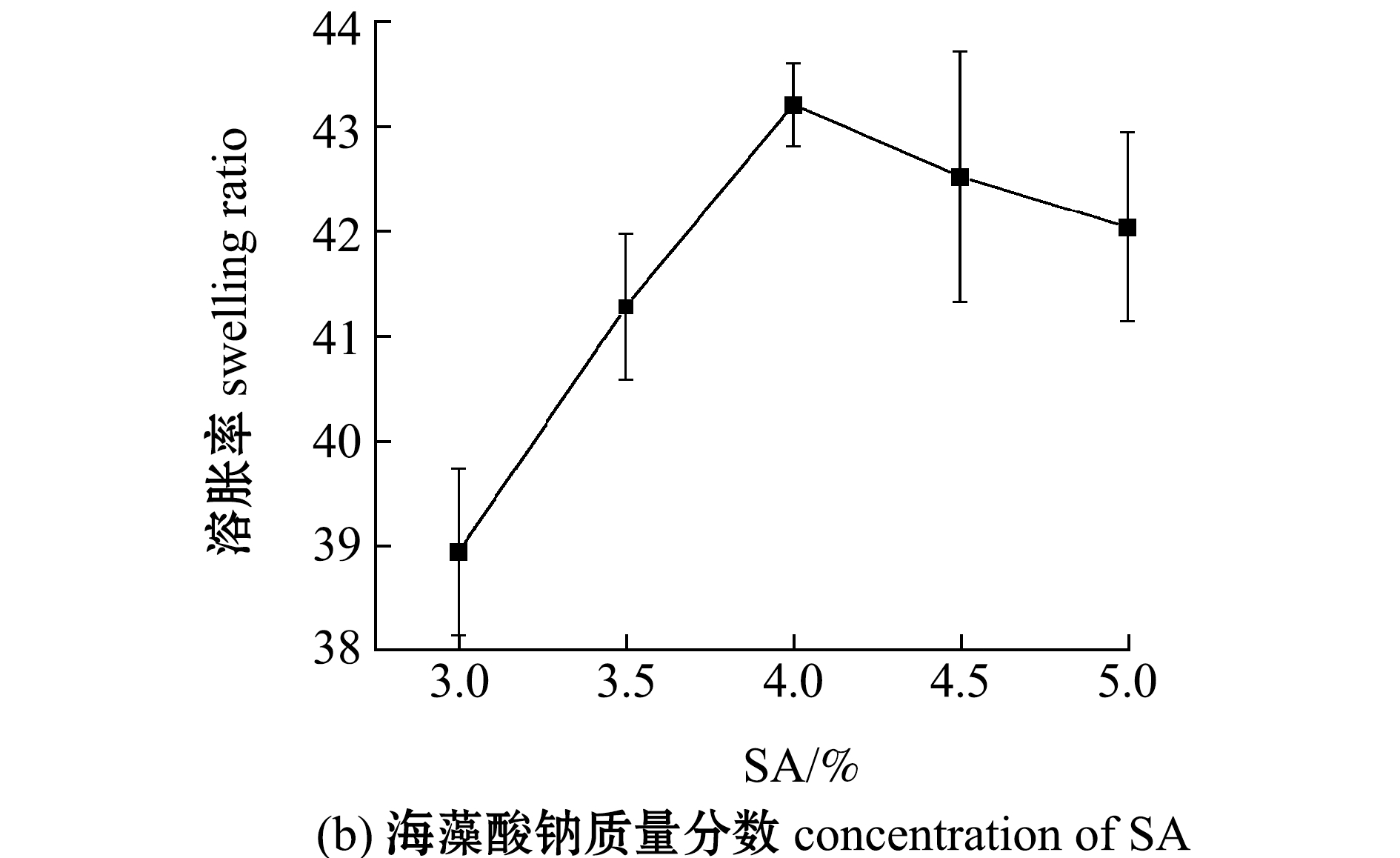
图3 淀粉、海藻酸钠质量分数对HIPS/SA凝胶溶胀率的影响
Fig.3 Effects of concentration of HIPS and SA aqueous solution on swelling ratio
2.3.2 海藻酸钠质量分数对HIPS/SA凝胶溶胀率的影响 从图3(b)可知,随着海藻酸钠质量分数的增加,HIPS/SA凝胶的溶胀率呈不断上升的趋势,在海藻酸钠质量分数达到4.0%~4.5%时,凝胶的溶胀率达到42.58~43.21,之后,随着HIPS质量分数的继续增加,凝胶的溶胀率迅速下降。这是因为在HIPS质量分数达到4.0%之前,随着海藻酸钠质量分数的增加,更多的海藻酸钠分子链交联形成最终网络结构,有利于提高凝胶的交联密度和凝胶中亲水基团的数量,使凝胶的溶胀率逐渐增加。但随着海藻酸钠质量分数的进一步增加,由于海藻酸钠内部氢键相互作用较大,此时海藻酸钠含量略有上升,就会使海藻酸钠溶液的黏度大幅增加,制备的凝胶交联密度过大,凝胶的溶胀率迅速下降。因此,本试验条件下,制备HIPS/SA凝胶的最佳海藻酸钠质量分数为4.0%~4.5%。
2.3.3 碱用量对HIPS/SA凝胶溶胀率的影响 从图4(a)可知,随着NaOH用量从240 μL逐渐增加至330 μL,凝胶的溶胀率呈不断上升的趋势,并在NaOH用量为300~330 μL时,凝胶的溶胀率达到43.35~43.69,之后,随着碱用量的继续增加,凝胶的溶胀率开始下降。这是因为随着碱用量增加,在NaOH的催化下,HIPS和海藻酸钠表面的氧负离子增多,有利于反应的进行,能促进凝胶的形成,提高凝胶的溶胀率。但随着碱用量的继续增加,过量的碱会使EDGE发生开环副反应,凝胶的交联密度降低,导致凝胶的溶胀率下降。因此,本试验条件下,制备HIPS/SA凝胶的最佳碱用量为300~330 μL。
2.3.4 EDGE用量对HIPS/SA凝胶溶胀率的影响
从图4(b)可见,随着EDGE用量从240 μL逐渐增加到300 μL,凝胶的溶胀率逐渐增加,并在300 μL时达到最大值(44.10)。这主要是因为交联剂EDGE用量的增加,单位体积内的EDGE分布也增多,因此,更容易形成交联网络。但随着交联剂量进一步增加,交联密度过大,三维网络结构过于致密,凝胶孔道数量增多,孔径变小,导致凝胶溶胀率下降。添加过量交联剂制得的凝胶,硬度更高,弹性更大,凝胶网络也变得更加紧密。因此,本试验条件下,制备HIPS/SA凝胶的最佳EDGE用量为300 μL。
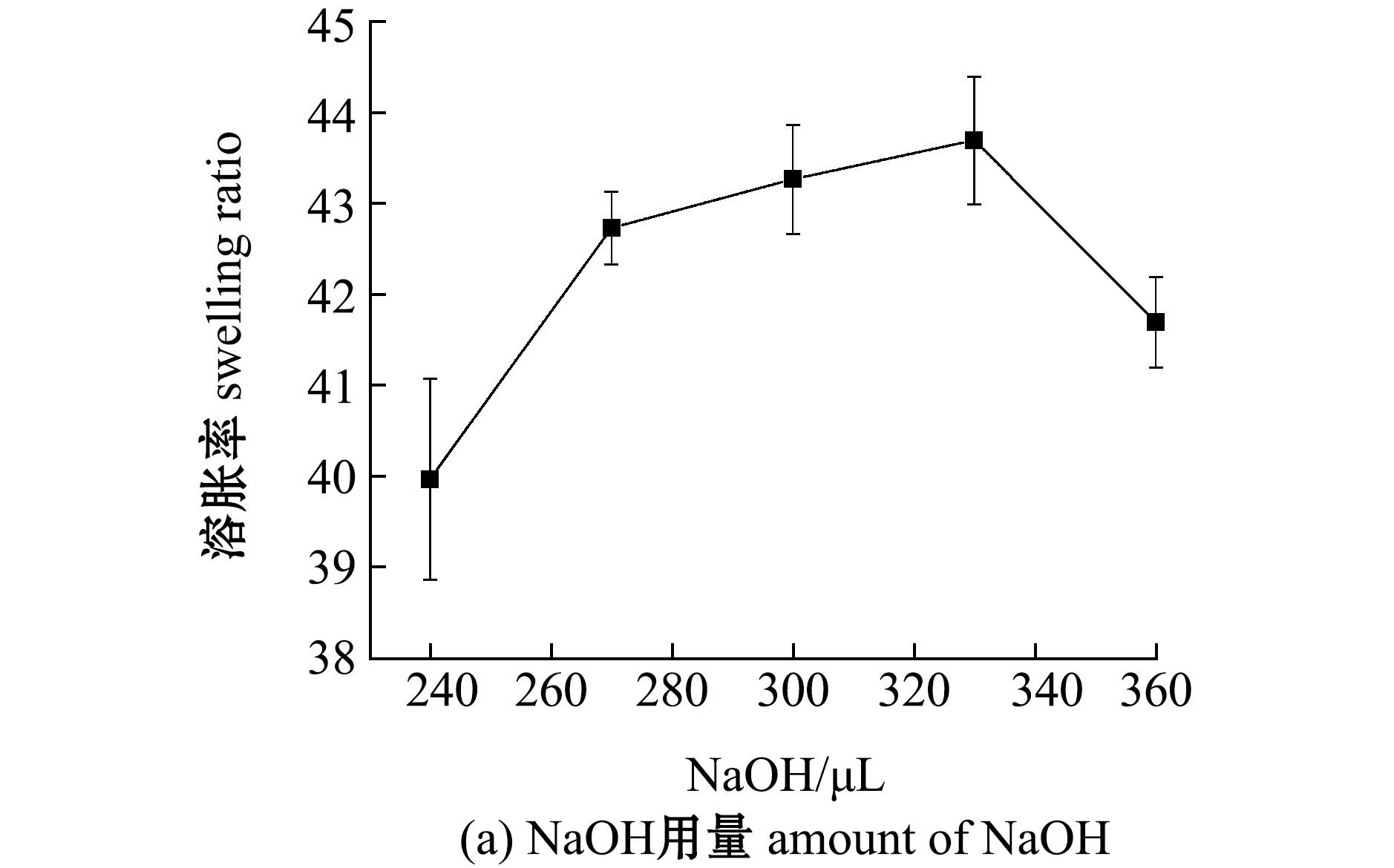
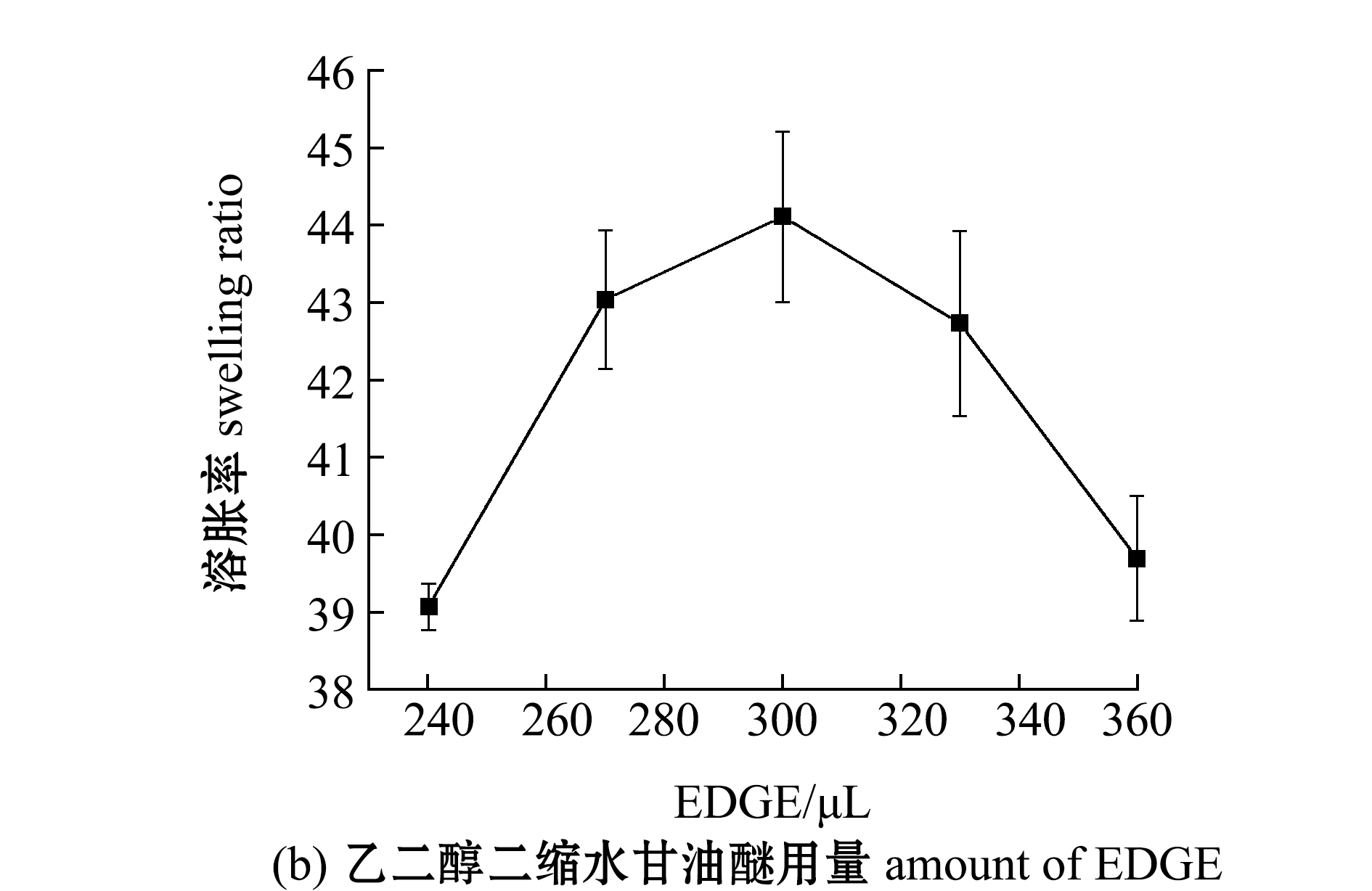
图4 NaOH、EDGE用量对HIPS/SA凝胶溶胀率的影响
Fig.4 Effects of amounts of NaOH and EDGE on swelling ratio
2.3.5 反应温度对HIPS/SA凝胶溶胀率的影响 从图5(a)可见,随着温度的逐渐增加,凝胶的溶胀率也呈不断上升的趋势,并在温度达到55 ℃时,溶胀率达到最大值(43.97),之后,随着温度的持续升高,凝胶的溶胀率出现下降趋势。这是因为温度增加,促进了HIPS和海藻酸钠交联网络结构的形成,凝胶的网络密度逐渐增加,保水性能得以增加,因此,凝胶的溶胀率逐渐增加。但随着温度的继续增加,凝胶的网络密度进一步增加,凝胶的网络结构变得十分紧密,且在高温下海藻酸钠有降解的可能,影响凝胶的吸水性能,导致凝胶的溶胀率下降。因此,本试验条件下,制备HIPS/SA凝胶的最佳反应温度为55 ℃。
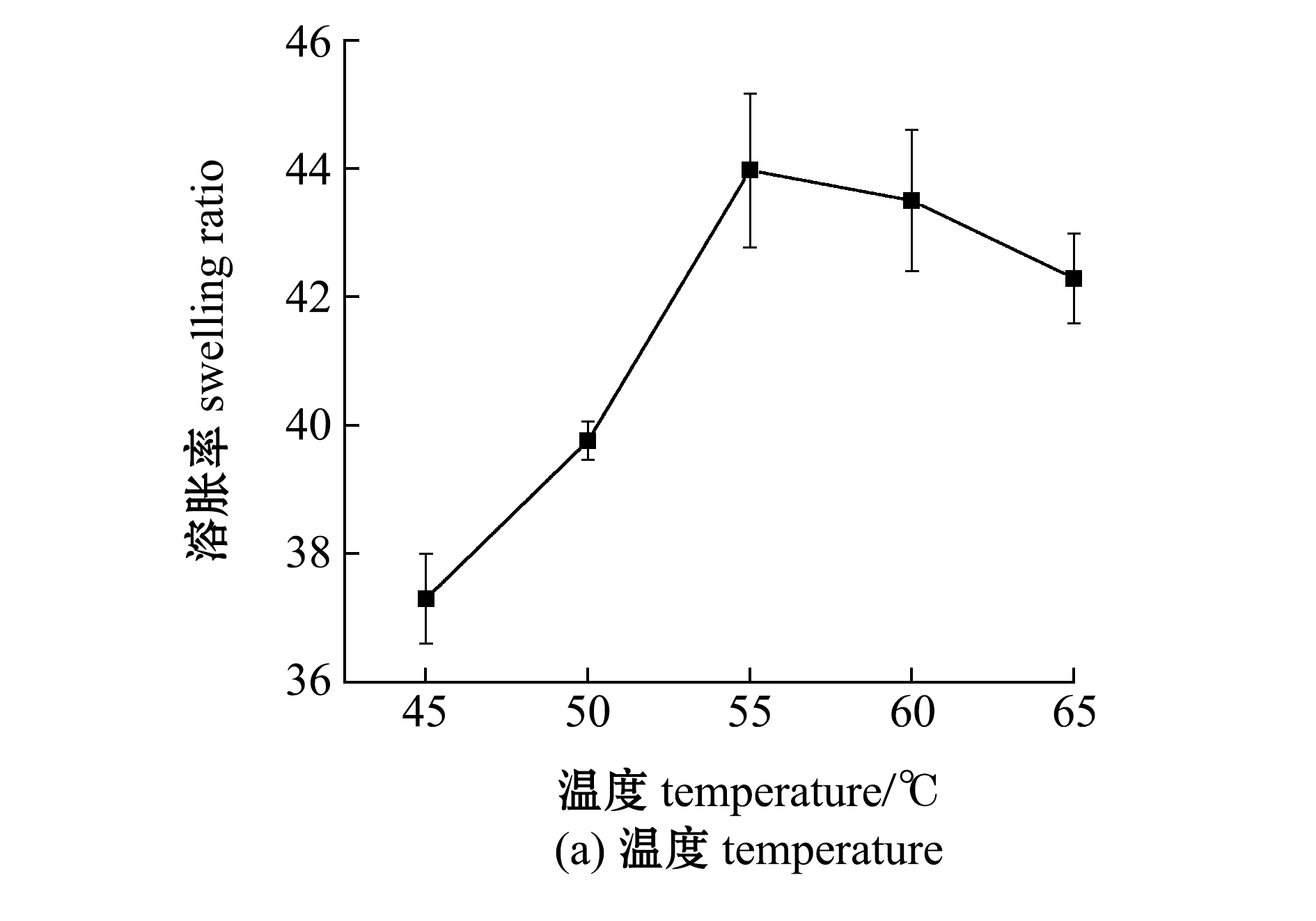
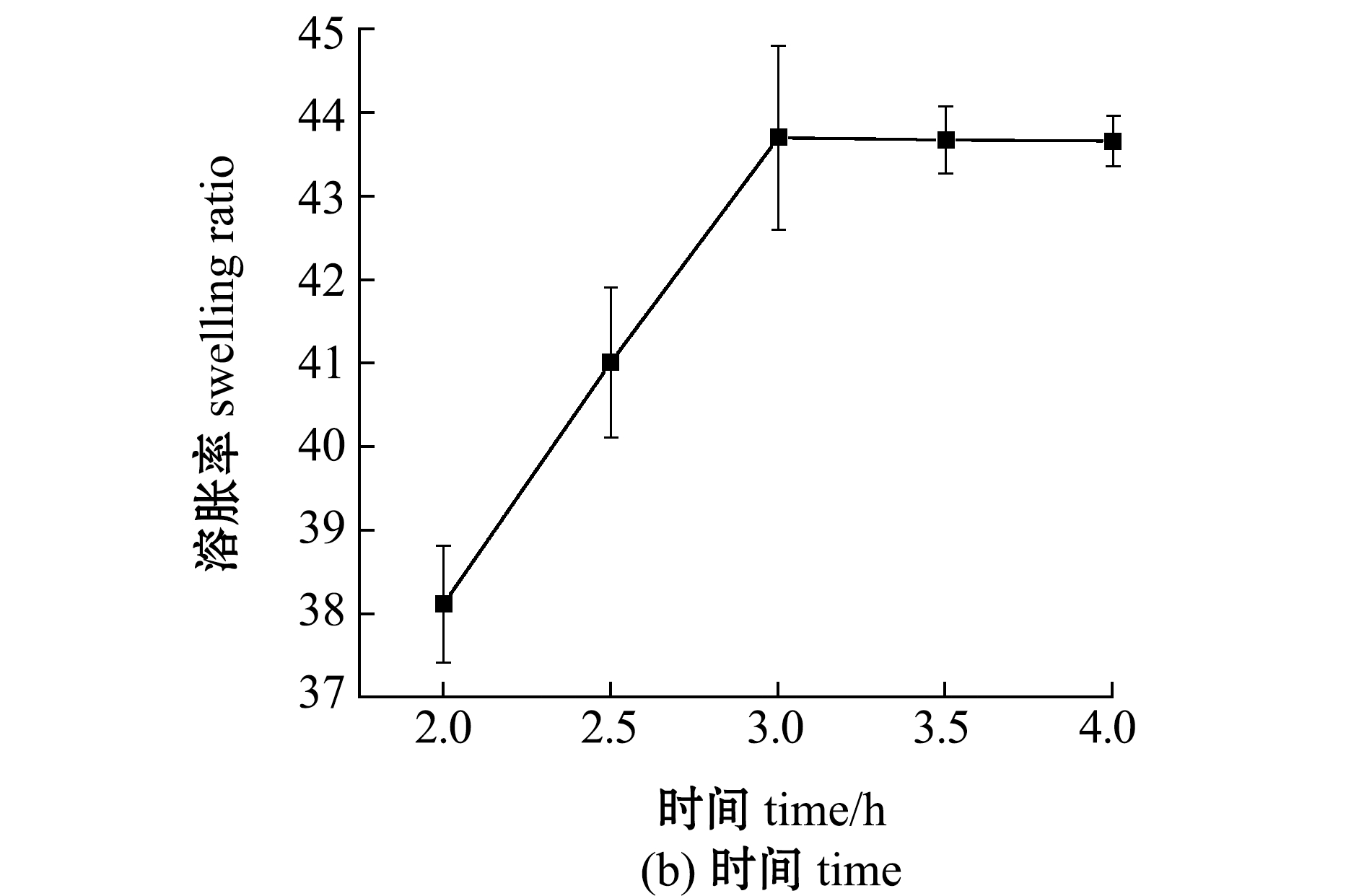
图5 反应温度和时间对HIPS/SA凝胶溶胀率的影响
Fig.5 Effects of reaction temperature and reaction time on swelling ratio
2.3.6 反应时间对HIPS/SA凝胶溶胀率的影响 从图5(b)可见,随着反应时间延长,凝胶的溶胀率呈先增加后平稳的变化趋势,在反应3 h时,凝胶的溶胀率达到最大值(43.69)。分析原因主要是随着反应时间的延长,更多的HIPS和海藻酸钠参与到反应中,凝胶的交联密度逐渐增加,溶胀率逐渐增加,随着反应时间的推移,反应逐渐达到平衡,凝胶溶胀率基本无变化。因此,本试验条件下,制备HIPS/SA凝胶的最佳反应时间为3 h。
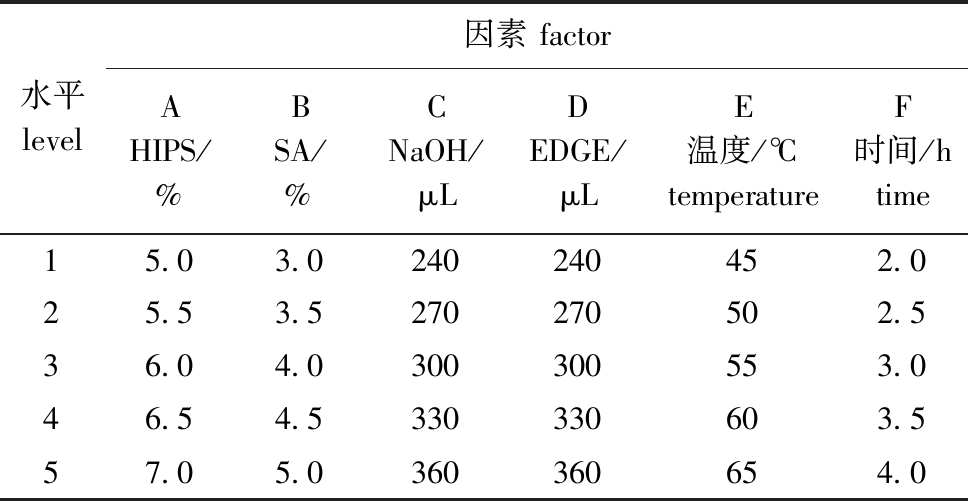
2.3.7 反应条件组合对HIPS/SA凝胶溶胀率影响的正交试验 为了确定HIPS/SA凝胶制备的最佳反应条件组合,以溶胀率为指标,设计了HIPS质量分数、海藻酸钠质量分数、NaOH用量、EDGE用量、反应温度、反应时间的6因素5水平L25(56)的正交试验,正交试验因素水平设计如表1所示,试验结果如表2所示。
表1 正交试验因素水平表
Tab.1 Factor and level table of orthogonal test
水平level因素factorAHIPS/%BSA/%CNaOH/μLDEDGE/μLE温度/℃temperatureF时间/htime15.03.0240240452.025.53.5270270502.536.04.0300300553.046.54.5330330603.557.05.0360360654.0
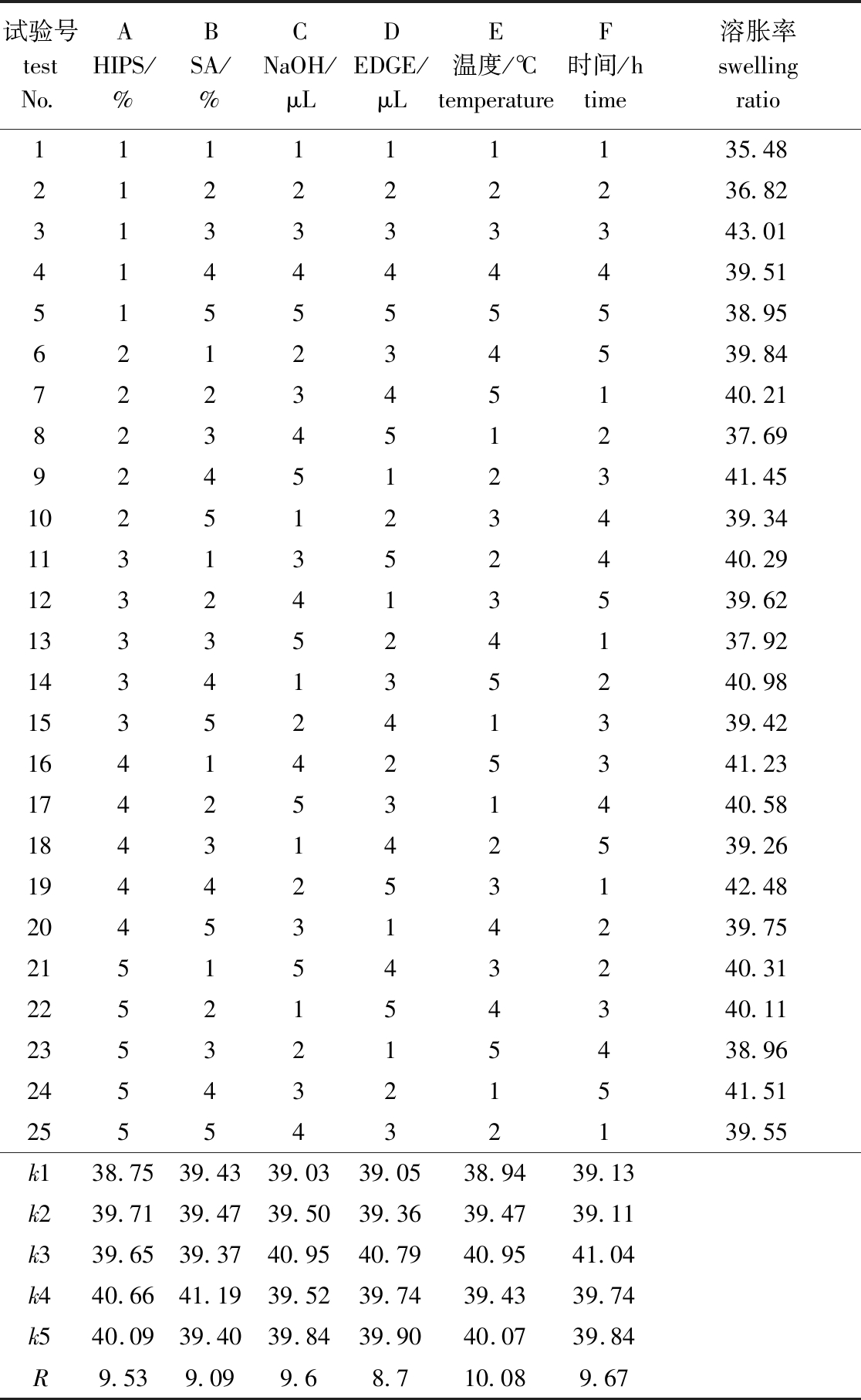
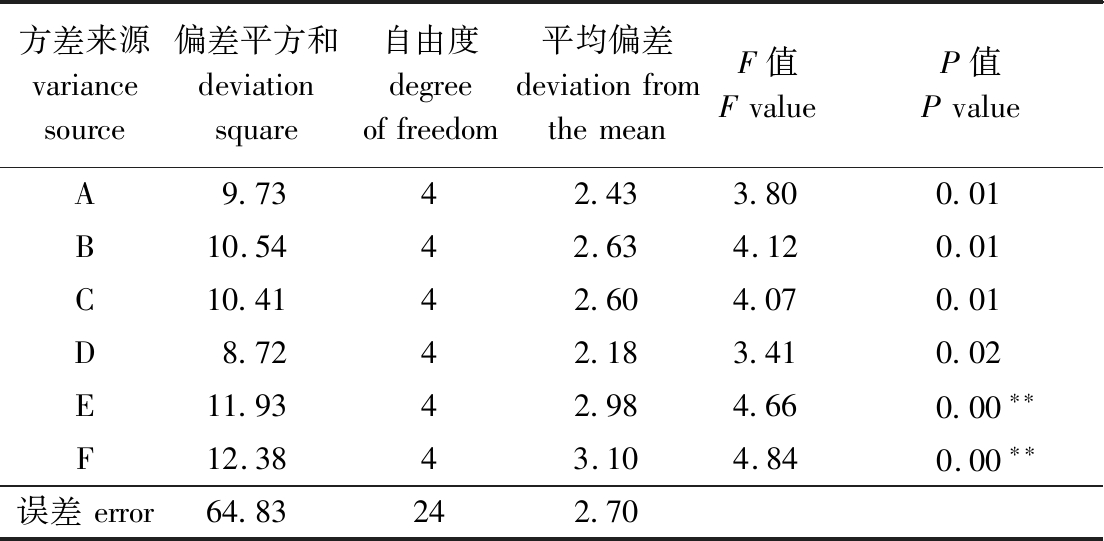
从表2可见,各反应条件对HIPS/SA凝胶溶胀率的影响因素依次为反应温度>反应时间>NaOH用量>HIPS质量分数>海藻酸钠质量分数>EDGE用量,正交试验的最佳试验组合为A4B4C3D3E3F3,即制备HIPS/SA凝胶的最佳条件为质量分数6.5%的HIPS 2 g、质量分数4.5%的海藻酸钠 2 g、NaOH用量300 μL、EDGE用量300 μL、反应温度55 ℃和反应时间3 h。在此最佳条件下进行验证试验,凝胶溶胀率可以达到44.20。方差分析显示,反应温度、反应时间均极显著影响HIPS/SA复合凝胶的溶胀率(P<0.01)(表3)。
表2 正交试验设计及试验结果
Tab.2 Design and results of orthogonal test
试验号testNo.AHIPS/%BSA/%CNaOH/μLDEDGE/μLE温度/℃temperatureF时间/htime溶胀率swellingratio111111135.48212222236.82313333343.01414444439.51515555538.95621234539.84722345140.21823451237.69924512341.451025123439.341131352440.291232413539.621333524137.921434135240.981535241339.421641425341.231742531440.581843142539.261944253142.482045314239.752151543240.312252154340.112353215438.962454321541.512555432139.55k138.7539.4339.0339.0538.9439.13k239.7139.4739.5039.3639.4739.11k339.6539.3740.9540.7940.9541.04k440.6641.1939.5239.7439.4339.74k540.0939.4039.8439.9040.0739.84R9.539.099.68.710.089.67
表3 正交试验结果的方差分析
Tab.3 Variance analysis of orthogonal test result
方差来源variancesource偏差平方和deviationsquare自由度degreeoffreedom平均偏差deviationfromthemeanF值FvalueP值PvalueA9.7342.433.800.01B10.5442.634.120.01C10.4142.604.070.01D8.7242.183.410.02E11.9342.984.660.00∗∗F12.3843.104.840.00∗∗误差error64.83242.70
注:**表示有极显著性影响(P<0.01)。
Note:** means very significant effect (P<0.01).
2.4 HIPS/SA凝胶的温度响应性能
图6A和图6B中的小图(数码图像)分别为HIPS/SA凝胶在20、50 ℃时收缩的图片。HIPS/SA凝胶表现出典型的温度响应特性,HIPS/SA凝胶的体积随温度升高发生了显著变化。为研究HIPS/SA凝胶在20、50 ℃下溶胀和收缩状态的微观结构差异,拍摄了HIPS/SA凝胶在20、50 ℃下的SEM图像。在20 ℃时,凝胶呈现多孔网络结构(图6A);在50 ℃时,凝胶孔洞收缩,凝胶表面变得相对光滑(图6B)。

图6 HIPS/SA凝胶在20 ℃(A)、50 ℃(B)的扫描电镜图片和凝胶图像
Fig.6 SEM images and photographs of HIPS/SA hydrogel at 20 ℃(A) and 50 ℃(B)
图7为HIPS/SA凝胶的VPTT曲线,HIPS/SA凝胶呈现明显的温度响应性能。随着温度升高,HIPS/SA凝胶的溶胀率缓慢下降,且在温度为20~35 ℃时下降幅度最大;温度较低时,HIPS/SA凝胶呈高度吸水溶胀状态,当温度超过35 ℃时,凝胶呈收缩状态,溶胀率显著降低;图中的拐点对应温度为34.9 ℃,即为HIPS/SA凝胶的VPTT。

图7 HIPS/SA凝胶的体积相转变温度曲线
Fig.7 VPTT curves of HIPS/SA hydrogel
3 讨论
3.1 HIPS/SA复合凝胶原材料的结构和资源优势
本研究中,选用天然生物质资源海藻酸钠和淀粉为主要原料,它们都是具有良好生物降解性、生物相容性的天然多糖,且无毒、易获取。淀粉分子链上含有活性较强的羟基,海藻酸钠分子结构中同样具有活性羟基和羧基,这些多糖中的活性基团为凝胶材料的合成提供了充足的活性位点,同时也为凝胶提供了有针对性的应用[23-26]。如羧基对金属离子具有良好的螯合性能,可作为金属离子的吸附位点;羟基能够提高多糖的水溶性,且可作为醚化和酯化反应的活性位点。本研究中,选用蜡质玉米淀粉为多支链结构,有利于制备多孔网络结构的凝胶材料。
3.2 HIPS/SA复合凝胶的原料组成和制备条件
目前,凝胶的应用主要集中在生物制药和食品工业领域,这些领域要求凝胶必须具有优异的生物相容性和生物降解性。然而,大多数凝胶是由石油基聚合物或单体制备,且反应条件较为苛刻,甚至需要高温、高压的反应条件。在这类凝胶的制备过程中,常使用有毒性的交联剂和单体,进而会增加凝胶的使用风险,缩小应用范围。本研究中,制备的HIPS/SA复合凝胶的原料主要由多糖(海藻酸钠和淀粉)、交联剂(乙二醇二缩水甘油醚和氯化钙)、催化剂(低含量氢氧化钠)组成,所有组分对生物和环境的潜在危害是极小的,特别是乙二醇二缩水甘油醚,它是一种对称型交联剂,由于其具有无毒、反应活性较强的优势,常作为生物医药凝胶的交联剂,上述制备凝胶所用原料可极大地提高凝胶的生物相容性,拓宽凝胶的应用范围。因此,制备HIPS/SA复合凝胶的原料组成具有较为明显的优势。
石油基类的凝胶通常在较高温度下的有机溶剂中进行交联反应,反应条件苛刻,同时产物也存在有机溶剂残留等问题。而在本研究中,以水作为溶剂,在55 ℃下反应3 h即可得到HIPS/SA复合凝胶产品,且HIPS/SA复合凝胶是通过温和的威廉逊(Williamson)醚化反应及钙离子的络合交联反应制备而成。选用乙二醇二缩水甘油醚和氯化钙作为混合交联剂,利用多糖与乙二醇二缩水甘油醚形成的共价键及与氯化钙形成配位键的双重交联方式制备多孔互穿网络的凝胶,相比于单一的离子键和共价键交联,这种多重交联方式使凝胶的温度响应性能更加优异,更容易形成交联网络结构。
3.3 HIPS/SA复合凝胶的温度响应性能
温度响应型凝胶是一类受到温度变化刺激后,其体积会发生明显变化的凝胶。从宏观角度来看,本研究中制备的HIPS/SA凝胶的温度响应性能,具体表现在其体积随温度而变化;从微观角度来看,凝胶的多孔结构随温度的变化而发生改变。体积相转变温度是衡量凝胶是否具有温度响应性能的重要参数,当温度低于体积相转变温度时,HIPS和海藻酸钠分子链上的羟基和羧基与水分子形成氢键,进而将大量的水分子锁在凝胶的多孔结构中;当温度高于体积相转变温度后,水分子与凝胶骨架间的氢键作用力减弱,部分水分子从凝胶骨架中脱除。相比其他合成聚合物型的温度响应凝胶,HIPS/SA凝胶不仅具有温度响应性能,而且还具有优异的生物相容性和生物降解性。因此,HIPS/SA凝胶在生物体内的药物控释领域具有良好的应用潜力,即在温度低于体积相转变温度时可装载药物,环境温度高于VPTT体积相转变温度时可实现药物的释放。
4 结论
1)本研究中得到制备HIPS/SA复合凝胶的最佳反应条件为质量分数6.5%的HIPS 2 g、质量分数4.5%的海藻酸钠2 g、NaOH用量300 μL、EDGE用量300 μL、反应温度55 ℃和反应时间3 h,其反应底物具有经济、无毒、活性高的优势,反应条件温和,反应容易发生。
2)本研究中制备的HIPS/SA复合凝胶,当温度低于复合凝胶的体积相转变温度VPTT时,凝胶呈溶胀状态,并呈现多孔网络结构;温度升高至VPTT(34.9 ℃)时,凝胶的溶胀率急剧下降,凝胶孔洞收缩。复合凝胶的体积和微观形貌随温度的改变呈现出较为明显的温度响应行为,表明HIPS/SA复合凝胶具有优异的温度响应性能。
[1] SHARIFZADEH G,HOSSEINKHANI H.Biomolecule-responsive hydrogels in medicine[J].Advanced Healthcare Materials,2017,6(24):1700801.
[2] NEZHAD-MOKHTARI P,GHORBANI M,ROSHANGAR L,et al.Chemical gelling of hydrogels-based biological macromolecules for tissue engineering:photo- and enzymatic-crosslinking methods[J].International Journal of Biological Macromolecules,2019,139:760-772.
[3] 于秋灵,李政,窦春妍,等.pH敏感性智能水凝胶的设计及其应用[J].化学进展,2020,32(sup 1):179-189.
YU Q L,LI Z,DOU C Y,et al.Design and application of pH sensitive and intelligent hydrogels[J].Progress in Chemistry,2020,32(sup 1):179-189.(in Chinese)
[4] LI X,SU X L.Multifunctional smart hydrogels:potential in tissue engineering and cancer therapy[J].Journal of Materials Chemistry B,2018,6(29):4714-4730.
[5] PEPPAS N A,KHARE A R.Preparation,structure and diffusional behavior of hydrogels in controlled release[J].Advanced Drug Delivery Reviews,1993,11(1/2):1-35.
[6] PEPPAS N A,VAN BLARCOM D S.Hydrogel-based biosensors and sensing devices for drug delivery[J].Journal of Controlled Release,2016,240:142-150.
[7] ZHANG M K,WANG J P,JIN Z Y.Supramolecular hydrogel formation between chitosan and hydroxypropyl β-cyclodextrin via Diels-Alder reaction and its drug delivery[J].International Journal of Biological Macromolecules,2018,114:381-391.
[8] 刘程,乔丽媛,柳承德,等.智能水凝胶及其在生物方向的应用[J].中国材料进展,2019,38(10):981-989,1016.
LIU C,QIAO L Y,LIU C D,et al.Intelligent hydrogels and their applications in biological fields[J].Materials China,2019,38(10):981-989,1016.(in Chinese)
[9] 王欣雅,吉木色,甘秋兰,等.IPN智能水凝胶药物缓释体系的设计及评价[J].材料科学与工程学报,2021,39(1):147-153.
WANG X Y,JI M S,GAN Q L,et al.Design and evaluation of IPN intelligent hydrogels for sustained and controlled drug delivery system[J].Journal of Materials Science and Engineering,2021,39(1):147-153.(in Chinese)
[10] KANAMALA M,WILSON W R,YANG M M,et al.Mechanisms and biomaterials in pH-responsive tumour targeted drug delivery:a review[J].Biomaterials,2016,85:152-167.
[11] 李子程,李攻科,胡玉玲.刺激响应聚合物在生物医药中的应用[J].化学进展,2017,29(12):1480-1487.
LI Z C,LI G K,HU Y L.Stimuli-responsive polymers in biomedical applications[J].Progress in Chemistry,2017,29(12):1480-1487.(in Chinese)
[12] 代明允,田野,刘鹰.2-羟基-3-丁氧基丙基羟乙基纤维素的制备及温度响应性能研究[J].大连海洋大学学报,2019,34(3):444-449.
DAI M Y,TIAN Y,LIU Y.Preparation and temperature response properties of 2-hydroxy-3-butoxypropyl hydroxyethyl cellulose[J].Journal of Dalian Ocean University,2019,34(3):444-449.(in Chinese)
[13] KLOUDA L.Thermoresponsive hydrogels in biomedical applications:a seven-year update[J].European Journal of Pharmaceutics and Biopharmaceutics,2015,97:338-349.
[14] HAO M A,SU Y L,WANG D J.Mechanical properties of PNIPAM based hydrogels:a review[J].Materials Science and Engineering:C,2017,70:842-855.
[15] PATRA P,RAMESHBABU A P,DAS D,et al.Stimuli-responsive,biocompatible hydrogel derived from glycogen and poly(N-isopropylacrylamide) for colon targeted delivery of ornidazole and 5-amino salicylic acid[J].Polymer Chemistry,2016,7(34):5426-5435.
[16] ZHUANG Y F,CHEN L W,ZHU Z Q,et al.Preparation and separation function of N-isopropylacrylamide copolymer hydrogels[J].Polymers for Advanced Technologies,2000,11(4):192-197.
[17] PAN C Y,LONG Q D,YU D,et al.Swelling and drug releasing properties of poly(N-isopropylacrylamide) thermo-sensitive copolymer gels[J].Frontiers of Chemistry in China,2008,3(3):314-319.
[18] 李启蒙,高灿柱,程终发.温度敏感性P(NtBA-co-AAm)聚合物和水凝胶的合成及表征[J].高分子材料科学与工程,2015,31(5):1-8.
LI Q M,GAO C Z,CHENG Z F.Synthesis and characterization of poly(N-tert-butylacrylamide-co-acrylamide)linear copolymer and hydrogels[J].Polymer Materials Science &Engineering,2015,31(5):1-8.(in Chinese)
[19] 代明允,田野,刘鹰,等.2-羟基-3-烯丙氧基丙基羟乙基纤维素的制备及温度敏感性能[J].精细化工,2019,36(4):595-601,608.
DAI M Y,TIAN Y,LIU Y,et al.Preparation and temperature responsive properties of 2-hydroxy-3-allyloxypropyl hydroxyethyl celluloses[J].Fine Chemicals,2019,36(4):595-601,608.(in Chinese)
[20] WANG Q,DU Y M,HU X W,et al.Preparation of alginate/soy protein isolate blend fibers through a novel coagulating bath[J].Journal of Applied Polymer Science,2006,101(1):425-431.
[21] ZHANG F J,CHENG G X,YING X G.Emulsion and macromolecules templated alginate based polymer microspheres[J].Reactive and Functional Polymers,2006,66(7):712-719.
[22] HORI Y,WINANS A M,IRVINE D J.Modular injectable matrices based on alginate solution/microsphere mixtures that gel in situ and co-deliver immunomodulatory factors[J].Acta Biomaterialia,2009,5(4):969-982.
[23] MOSHAVERINIA A,CHEN C,AKIYAMA K,et al.Alginate hydrogel as a promising scaffold for dental-derived stem cells:an in vitro study[J].Journal of Materials Science Materials in Medicine,2012,23(12):3041-3051.
[24] ABASALIZADEH F,MOGHADDAM S V,ALIZADEH E,et al.Correction to:alginate-based hydrogels as drug delivery vehicles in cancer treatment and their applications in wound dressing and 3D bioprinting[J].Journal of Biological Engineering,2020,14:17.
[25] VARAPRASAD K,JAYARAMUDU T,KANIKIREDDY V,et al.Alginate-based composite materials for wound dressing application:a mini review[J].Carbohydrate Polymers,2020,236:116025.
[26] WANG Y Q,FENG Y,ZHANG X F,et al.Alginate-based attapulgite foams as efficient and recyclable adsorbents for the removal of heavy metals[J].Journal of Colloid and Interface Science,2018,514:190-198.