新鲜罗非鱼组织含水量高,在微生物和酶的作用下,极易发生腐败变质,将其进行干燥处理可保持鱼肉品质[1],但不同干燥方式制得的干制品品质存在一定差异,干制罗非鱼片组织中存在一定空隙的孔径,在贮藏过程中极易受潮发生霉变,从而缩短货架期。为了提高干制罗非鱼片的品质,延长其贮藏期,有必要了解干制罗非鱼片的解吸-吸附性质与其平衡含水率和水分活度间的关系,并有效控制干制罗非鱼片的平衡含水率与水分活度。水分活度是指在密闭空间中,食品的平衡蒸气压与同一温度下纯水的饱和蒸气压比值[2],其代表食品中的自由水能被微生物和生化反应利用的程度[3]。解吸-吸附等温线表示在一定温度条件下,平衡含水率与水分活度间的变化关系,可为物料干燥工艺的优化及物料的贮藏条件提供参考,并为确定物料的贮藏期提供一定的理论依据[4-5]。以不同温度条件下的解吸-吸附等温线数据为基础可计算出一些热力学函数,如净等量吸附热、净等量解吸热和微分熵等,了解这些热力学特性可为物料的加工及贮藏工艺条件的设置提供参考。
目前,国内外学者已开展了食品解吸、吸附特性等诸多研究[6-8],但主要集中在农产品中,如龙眼[9]、小麦[10]、葡萄籽[11]等,而对其在水产品中的研究较少,特别对罗非鱼平衡含水率规律的研究尚不多见,但也有一些有关新鲜鱼肉的解吸规律及在干燥过程中罗非鱼肉平衡含水率的变化与解吸规律的研究报道。Ponwiboon等[12]采用静态称量法研究了不同条件下制得的罗非鱼片在不同温度和相对湿度条件下的解吸等温线,并采用5种模型对解吸等温线进行拟合,发现Oswin模型是描述解吸等温线的最佳模型。关志强等[13]采用静态称量法研究了干燥过程中罗非鱼肉的平衡含水率模型,通过对试验数据的拟合,发现Oswin 修正模型是描述罗非鱼肉的平衡含水率曲线的最佳模型。段振华等[14]研究了新鲜罗非鱼肉在60 ℃条件下的解吸平衡含水率,并对其进行回归分析,发现Chung-Pfost 模型是描述解吸平衡含水率的最佳模型。
真空冷冻-热泵联合干燥技术结合了两种干燥方式的优势,其干燥罗非鱼片的品质高于独立热泵干燥罗非鱼片品质,接近真空冷冻干燥罗非鱼片品质[15],且干燥时间也能缩短。食品热力学特性分析可提供解吸-吸附过程中水分的特性和能量需求信息,有利于食品加工工艺的优化和适宜贮藏环境的选择,可为解决干燥、流通和贮藏工艺条件的设计问题提供理论依据。不同干燥方式和干燥工艺对解吸-吸附曲线存在一定的影响,由于不同干燥方式对罗非鱼片的结构影响程度不同,作者在前期研究中曾得出基于真空冷冻-热泵联合干燥罗非鱼片品质最佳的结论[15]。本研究中,采用预处理结合真空冷冻-热泵联合干燥的罗非鱼片为原料,研究其在25、35、45 ℃时和水分活度(aw)为0.111 6~0.843 4时的解吸-吸附等温线,并选取8种常见的数学模型对解吸-吸附等温线数据进行拟合,通过研究基于真空冷冻-热泵联合干制鱼片的解吸-吸附等温线及热力学特性,以期为其干燥和贮藏条件的选择,以及罗非鱼片加工工艺的优化和贮藏期的延长提供参考。
1 材料与方法
1.1 材料
试验用鲜罗非鱼购自广东省湛江市湖光市场,取罗非鱼背部两侧部分,切成规格为100 mm×50 mm×5 mm的罗非鱼片,质量约为30 g。
试验试剂:氯化锂、氯化镁、溴化钠、氯化铜、氯化钠、氯化钾、麝香草酚(均为分析纯),均购于湛江科铭科技有限公司。
主要仪器设备:热泵干燥装置,试验室自行搭建(图1);KQ-500DE数控超声波清洗器(昆山市超声仪器有限公司);LGJ-10E 型冷冻干燥机(北京四环科学仪器厂有限公司)。
1.2 方法
1.2.1 吸附等温线样品的制作 前期试验发现,罗非鱼片经超声波辅助聚葡萄糖渗透预处理结合真空冷冻-热泵联合干燥后,其品质比独立热泵干燥罗非鱼片的品质高,本试验中采用前期试验获得的超声波辅助聚葡萄糖渗透预处理最佳工艺条件制作试验原料。具体工艺如下:将鱼片浸渍于80 g/L聚葡萄糖+30 g/L氯化钠混合溶液中,采用450 W超声波仪器超声65 min,后置于冷阱(温度-60 ℃)条件下预冻2 h(直到其中心温度达到-20 ℃),然后放置在隔板温度为36 ℃、真空度为10 Pa以下条件进行真空冷冻干燥5 h,最后转移到温度为45 ℃、风速为2.5 m/s的热泵装置中进行热泵干燥,当干基含水量降为(0.30±0.02)g/g时,停止干燥[15]。使用P2O5将干制罗非鱼片水分调节至5%,采用高速万能粉碎机将其粉碎成均匀的粉末,并采用密封袋包装置于干燥环境中保存备用。
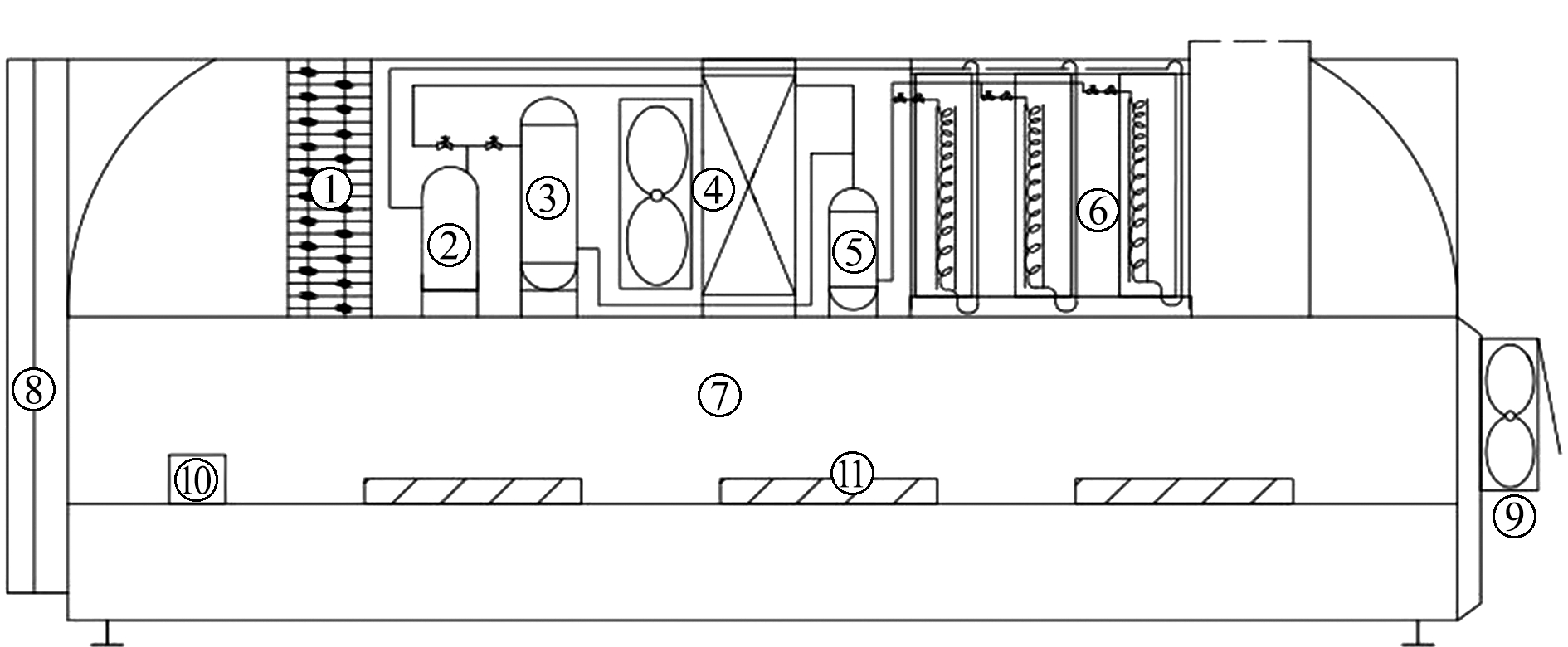
① 辅助加热器;② 压缩机;③ 水冷冷凝器;④ 冷风冷凝器;⑤ 贮液罐;⑥ 蒸发器;⑦ 干燥箱;⑧ 活动门;⑨ 排气扇; ⑩ 温度、湿度和风速探头;  测试材料。
测试材料。
① auxiliary heater;② compressor;③ water-cooled condenser;④ wind condenser; ⑤ liquid storage tank;⑥ evaporator;⑦ drying box;⑧ movable door;⑨ exhale fan;⑩ temperature, humidity, and wind speed test probes; test material.
test material.
图1 热泵干燥装置
Fig.1 Heat pump drying device
1.2.2 解吸等温线样品的制作 将干制罗非鱼片置于相对湿度为90%、温度为10 ℃的人工气候箱中并定期翻转,当其干基含水率达84%左右时,将其粉碎并采用密封袋包装,置于4 ℃冰箱中平衡24 h后进行解吸试验。
1.2.3 罗非鱼片干制品安全含水率 水分是微生物繁殖和物料内各种化学和生物化学反应的必要条件,罗非鱼片干制品的微生物生长繁殖取决于水分活度。当aw=0.65~0.70时,霉菌、酵母菌和细菌生长受到抑制;当aw=0.60~0.65时,物料内的微生物生长繁殖完全受到抑制;随着aw下降,当aw<0.60时,几乎所有微生物均无法生存[16]。故将aw=0.60时对应的平衡含水率称为罗非鱼片干制品贮藏的绝对安全含水率,将aw=0.70时对应的平衡含水率称为罗非鱼片干制品贮藏的相对安全含水率。根据25、35、45 ℃条件下,罗非鱼片干制品的吸附和解吸试验值拟合出最佳模型,计算物料的相对和绝对安全含水率。
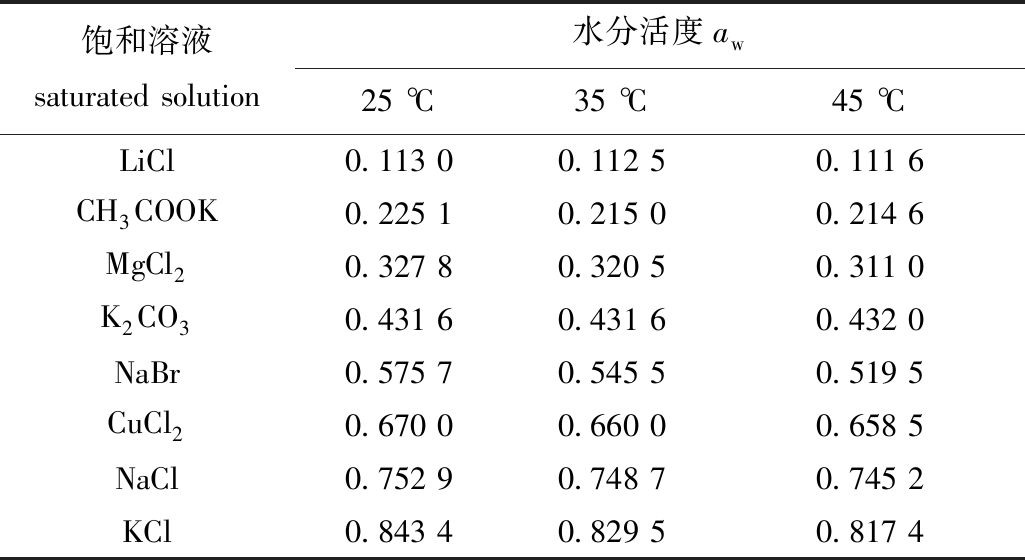
1.2.4 罗非鱼片干制品吸附平衡含水率测定 采用静态称量法测定罗非鱼片干制品在25、35、45 ℃时和水分活度为0.111 6~0.843 4(表1[17-18])时的平衡含水率,平衡相对湿度(ERH)与水分活度(aw)的换算公式为ERH=aw×100%。
表1 饱和盐溶液在不同温度下的水分活度
Tab.1 Relative water activity of saturated salt solution at different temperatures
饱和溶液saturatedsolution水分活度aw25℃35℃45℃LiCl0.11300.11250.1116CH3COOK0.22510.21500.2146MgCl20.32780.32050.3110K2CO30.43160.43160.4320NaBr0.57570.54550.5195CuCl20.67000.66000.6585NaCl0.75290.74870.7452KCl0.84340.82950.8174
试验前将装有配制好饱和盐溶液的干燥器置于试验所需温度恒温箱24 h,使干燥器内的饱和溶液达到平衡,在装有水分活度大于0.75的饱和溶液干燥器内加入0.2 g左右麝香草酚以抑制微生物生长。称取1.0 g干制罗非鱼粉置于称量瓶,每隔12 h称量其质量,称量后均匀搅拌样品,并将称量瓶快速转移至干燥器。当前后两次质量小于0.003 g时,即认为样品到达吸湿平衡,结束试验,并测量此时样品含水率。每组试验设3个平行,结果取其平均值。
1.2.5 罗非鱼片干制品解吸平衡含水率测定 解吸试验的称量方法及平衡判断方法与上述罗非鱼片干制品吸附平衡含水率测定方法相同。
1.2.6 解吸和吸附模型 结合国内外有关食品解吸-吸附数学模型研究[19-21],选取8种常见的数学模型对罗非鱼片干制品的解吸-吸附等温线数据进行拟合,模型及表达式如表2所示。
表2 拟合的干制罗非鱼粉解吸-吸附等温线模型
Tab.2 Model of fitting desorption-adsorption isotherm of dried tilapia meal

序号No.模型model表达式expression1SmithMe=a+bln(1-aw)2ModifiedHendersonMe=-ln(1-aw)a(t+c)[]1b3GABMe=m0ckaw(1-kaw)(1-kaw+kcaw)4BETMe=m0caw(1-aw)[1+(c-1)aw]5HendersonMe=-ln(1-aw)a[]1b6OswinMe=aaw1-aw()b7HalseyMe=-alnaw()1b8PelegMe=m1an1w+m2an2w
注:Me—平衡含水率;m0—单分子含水值;t—温度;a、b、c、k、m1、m2、n1、n2均为模型参数。
Note:Me—equilibrium moisture; m0—single-molecule moisture; t—temperature; a,b,c,k,m1,m2,n1 and n2,model parameters.
1.2.7 净等量吸附热、解吸热及微分熵 净等量吸附热是指在一定温度和水分活度下,水蒸气分子在物料表面吸附过程中所释放的能量,其大小可反映水分子与固体基质间束缚力的强弱。在一定水分活度下,通过克劳修斯-克拉贝龙(Clausius-Clayperon)公式求出净等量吸附热或解吸热(qst)[22]:
![]()
(1)
其中: qst为净等量吸附热或解吸热(kJ/mol);R为通用气体常数[8.314 J/(mol·K)];T为绝对温度(K);aw为水分活度;x为平衡含水率(%)。由式(1)可知,qst可通过lnaw与1/T线性拟合所得直线的斜率确定。
微分熵(Sd,J/(mol·K))能反映吸附质与固体基质表面间的活性位点,其与固体基质表面的水分可吸附性位点成正比,通过Sd可了解物料内部结构。在热力学体系中,Sd与qst的函数关系[23]为
(lnaw)x=-qst/(RT)+Sd/R。
(2)
由式(2)可知,Sd可通过以lnaw与1/T线性拟合所得直线的截距确定。
1.2.8 熵-焓互补理论 本研究中,运用熵-焓互补理论,评价罗非鱼片干制品水分吸附过程中发生的物理化学现象,以及该过程中焓与熵的变化规律,从而确定罗非鱼片干制品水分驱动机理。在特定的含水率条件下,qst与Sd呈线性关系,其计算公式为[24]
qst=TβSd+ΔGβ。
(3)
其中: Tβ为等速温度(K),表示在水分吸附过程中,当所有化学反应的反应速度相等时所对应的温度;ΔGβ为Tβ时的吉布斯自由能(kJ/mol)。
为了进一步验证熵-焓互补理论,Krug等[25]建议采用调和平均温度Thm和Tβ进行比较。Thm表达式为
![]()
(4)
其中: n为等温线的数量,当Thm≠Tβ时才存在熵-焓互补理论,若Tβ>Thm吸附过程为焓驱动,若Tβ<Thm吸附过程为熵驱动。
1.3 数据处理
试验数据均采用3次平行试验的平均值,采用JMP Pro 13.0软件进行回归分析。
2 结果与分析
2.1 贮藏温度对罗非鱼片干制品吸附和解吸等温线的影响
图2为不同温度条件下罗非鱼片干制品的吸附等温线和解吸等温线,根据国际理论和应用化学联合会(International Union of Pure and Applied Chemistry,IUPAC)规定的分类方法,罗非鱼片干制品的吸附等温线和解吸等温线都属于Ⅲ型等温线。按照Lahsasni等[26]对水分活度的分类,水分活度被分为3部分:Ⅰ区间水分为单分子层状态(aw =0.1~0.3),Ⅱ区间水分为多分子层状态(aw =0.3~0.7),Ⅲ区间水分为游离水状态(aw =0.7~1.0)。由图2可知,当aw<0.5时,吸附等温线和解吸等温线增加较缓慢。由图2A可知,罗非鱼片干制品吸附过程中,在相同水分活度条件下,温度越低物料所含的平衡含水率越高,说明干制品的复水率与温度并不呈正相关性,这为干制品复水加工提供一定的参考依据;此外,在相同aw条件下,35、45 ℃下的吸附等温线几乎重合,由此可见,温度对样品吸附能力影响不大,这为干制品的贮藏温度提供了实际参考依据。由图2B可知,干制品解吸过程中,当aw<0.5时,平衡含水率缓慢上升,说明在该干燥阶段需要提供较大的能量;aw>0.5时平衡含水率快速上升,说明在该阶段物料组织内所含水分主要是多分子层中有溶解能力及可移动的水分和自由水,在干燥过程中易被除去,这可为罗非鱼片干燥工艺优化提供参考依据。
从图2还可见:在相同水分活度下,罗非鱼片干制品的吸附等温线和解吸等温线均随温度上升呈下降趋势,但在不同温度条件下,罗非鱼片干制品的平衡含水率较为接近;而平衡含水率随着水分活度的增大不断增大,其对应的平衡含水率增加幅度大于由温度变化引起的增加幅度。由此可见,在一定水分活度范围内,水分活度是影响吸附等温线和解吸等温线的主要因素。
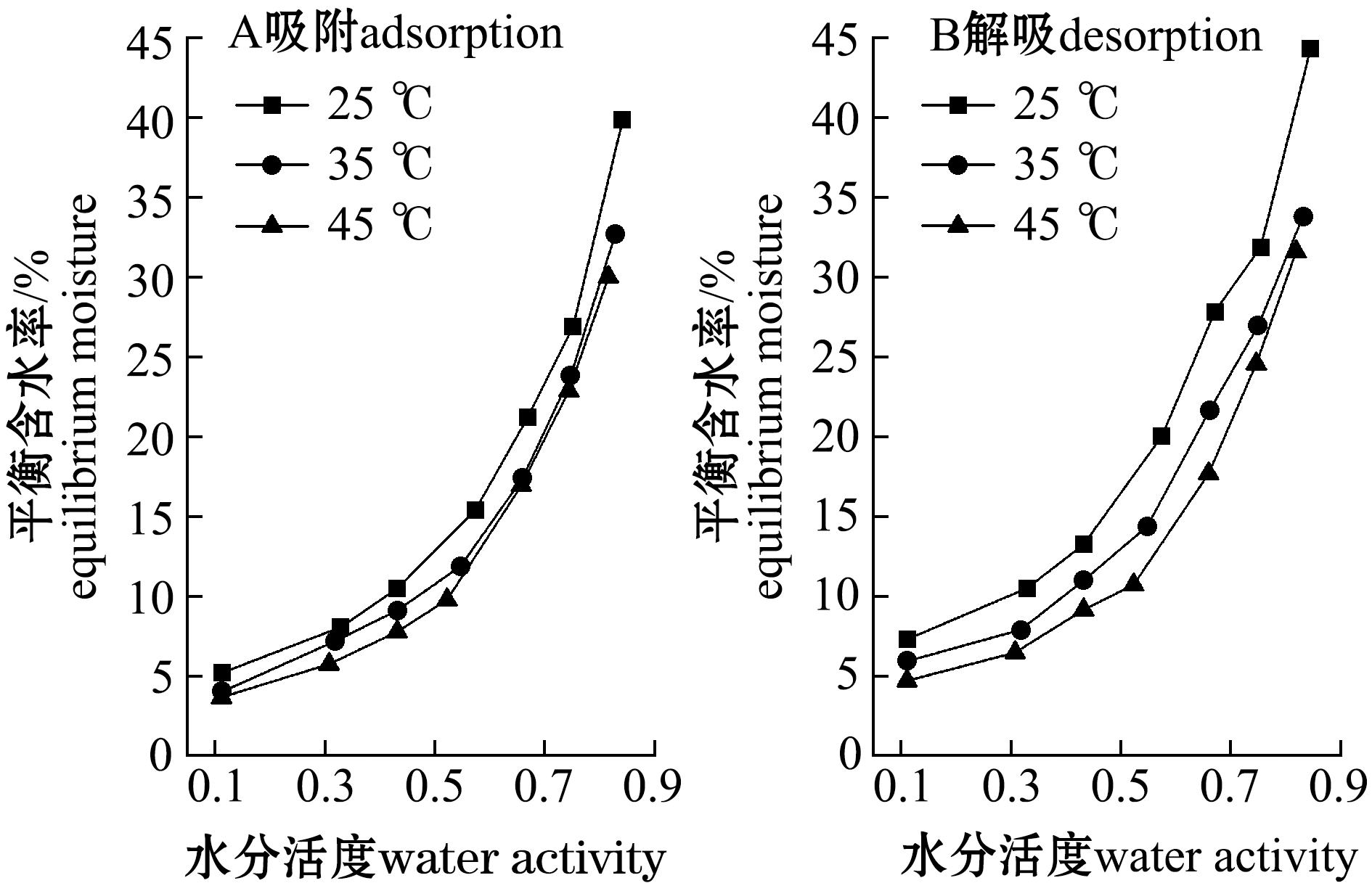
图2 不同温度下罗非鱼片干制品的吸附和解吸等温线
Fig.2 Adsorption isotherms and desorption isotherms of dried tilapia fillets under different temperature conditions
从图3可见:在整个水分活度范围内,罗非鱼片干制品的解吸和吸附过程均存在滞后现象,但随着温度增加,滞后现象越无明显差异;在45 ℃条件下,解吸等温线和吸附等温线几乎重合,而当罗非鱼片干制品处于25 ℃条件下时,解吸等温线和吸附等温线具有明显差异,可见温度与滞后现象有着密切的联系。

图3 罗非鱼片干制品在不同温度条件下的吸附和解吸等温线比较
Fig.3 Comparison of adsorption and desorption isotherms of dried tilapia fillets under different temperature conditions
2.2 吸附与解吸模型的拟合与分析
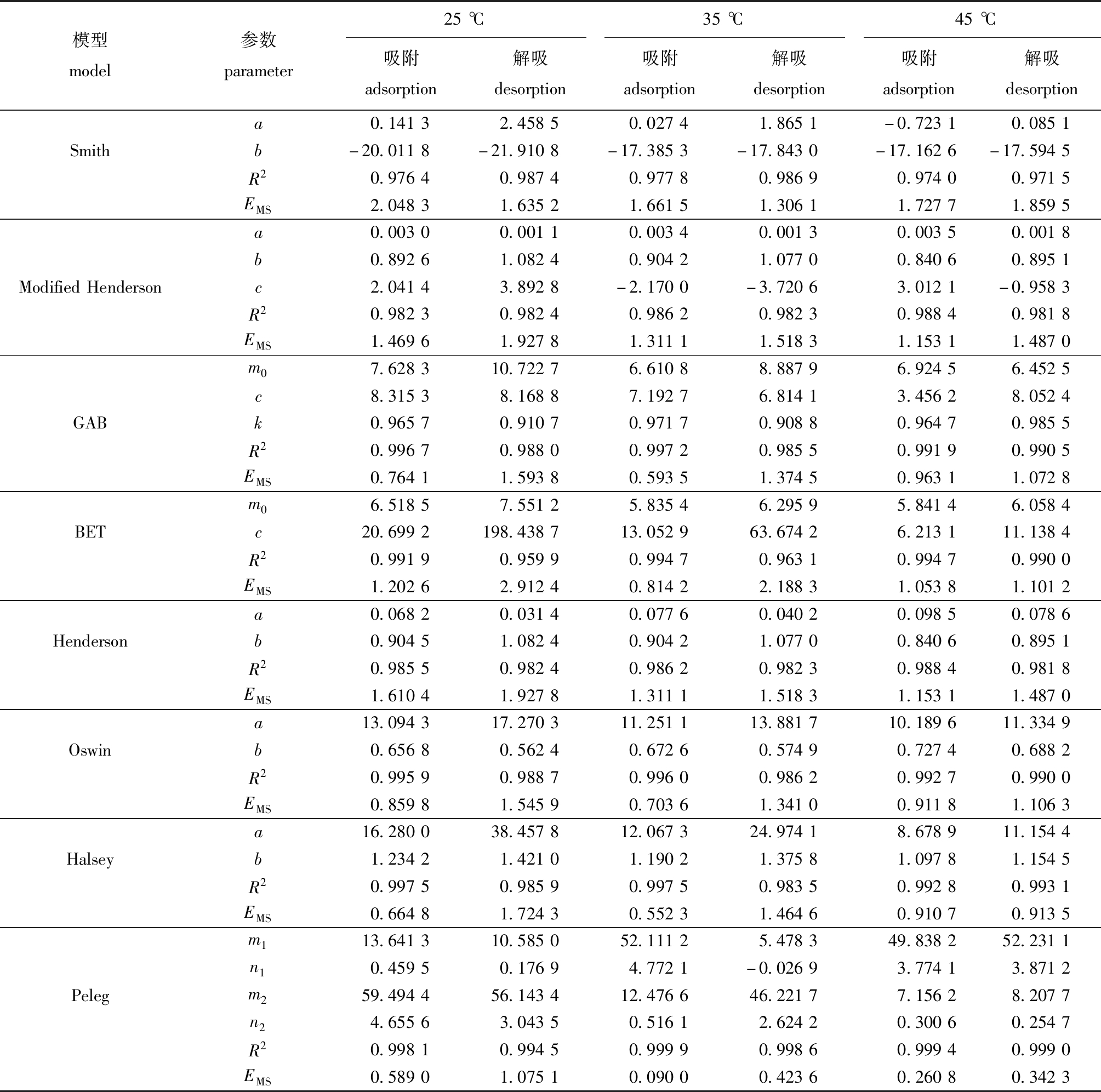
根据罗非鱼片干制品解吸和吸附过程所得的平衡含水率试验值和水分活度数值,采用JMP Pro13.0软件对8种常见的数学模型进行非线性拟合,各模型的参数及评价指标如表3所示。
由表3可知,25、35、45 ℃条件下,根据罗非鱼片干制品的吸附和解吸试验值拟合出的Peleg模型决定系数(R2)最大且均方误差(EMS)值最小,从而确定Peleg模型是描述罗非鱼片干制品吸附和解吸特性的最佳模型。将Peleg模型的m1、n1、m2、n2表示为温度的多项式aT2+bT+c进行非线性拟合,可得吸附过程中各参数与温度的关系为
表3 各模型的评价值
Tab.3 Evaluation value of each model
模型model参数parameter25℃35℃45℃吸附adsorption解吸desorption吸附adsorption解吸desorption吸附adsorption解吸desorptiona0.14132.45850.02741.8651-0.72310.0851Smithb-20.0118-21.9108-17.3853-17.8430-17.1626-17.5945R20.97640.98740.97780.98690.97400.9715EMS2.04831.63521.66151.30611.72771.8595a0.00300.00110.00340.00130.00350.0018b0.89261.08240.90421.07700.84060.8951ModifiedHendersonc2.04143.8928-2.1700-3.72063.0121-0.9583R20.98230.98240.98620.98230.98840.9818EMS1.46961.92781.31111.51831.15311.4870m07.628310.72276.61088.88796.92456.4525c8.31538.16887.19276.81413.45628.0524GABk0.96570.91070.97170.90880.96470.9855R20.99670.98800.99720.98550.99190.9905EMS0.76411.59380.59351.37450.96311.0728m06.51857.55125.83546.29595.84146.0584BETc20.6992198.438713.052963.67426.213111.1384R20.99190.95990.99470.96310.99470.9900EMS1.20262.91240.81422.18831.05381.1012a0.06820.03140.07760.04020.09850.0786Hendersonb0.90451.08240.90421.07700.84060.8951R20.98550.98240.98620.98230.98840.9818EMS1.61041.92781.31111.51831.15311.4870a13.094317.270311.251113.881710.189611.3349Oswinb0.65680.56240.67260.57490.72740.6882R20.99590.98870.99600.98620.99270.9900EMS0.85981.54590.70361.34100.91181.1063a16.280038.457812.067324.97418.678911.1544Halseyb1.23421.42101.19021.37581.09781.1545R20.99750.98590.99750.98350.99280.9931EMS0.66481.72430.55231.46460.91070.9135m113.641310.585052.11125.478349.838252.2311n10.45950.17694.7721-0.02693.77413.8712Pelegm259.494456.143412.476646.22177.15628.2077n24.65563.04350.51612.62420.30060.2547R20.99810.99450.99990.99860.99940.9990EMS0.58901.07510.09000.42360.26080.3423
m1=-0.203 7T2+16.07T-260.7,
n1=-0.026 6T2+2.024 4T-33.556,
m2=0.208 5T2-17.211T+359.47,
n2=0.019 6T2-1.591 2T+32.172。
将参数代入方程![]() 得
得
Me=(-0.203 7T2+16.07T-260.78)×
aw(-0.026 6T2+2.024 4T-33.556)+(0.208 5T2-
17.211T+359.47)×aw(0.019 6T2-1.591 2T+32.172)。
解吸过程中各参数与温度的关系为
m1=0.259 3T2-16.069T+250.24,
n1=0.020 5T2-1.251T+18.632,
m2=-0.140 5T2+7.435 5T-41.956,
n2=-0.009 8T2+0.543 1T-4.440 4。
将参数代入方程![]() 得
得
Me=(0.259 3T2-16.069T+250.24)×
aw(0.020 5T2-1.251T+18.632)+(-0.140 5T2+7.435 5T-
41.956)×aw(-0.009 8 T2+0.543 1T-4.440 4)。
将3个温度分别代入Peleg数学模型中可得出系列吸附方程和解吸方程分别为
![]() (25 ℃吸附),
(25 ℃吸附),
![]() (25 ℃解吸),
(25 ℃解吸),
![]() (35 ℃吸附),
(35 ℃吸附),
![]() (35 ℃解吸),
(35 ℃解吸),
![]() (45 ℃吸附),
(45 ℃吸附),
![]() (45 ℃解吸)。
(45 ℃解吸)。
为了验证Peleg数学模型的准确性和可靠性,将罗非鱼片干制品的平衡含水率试验值和通过Peleg数学模型所得的预测值进行比较,结果如图4所示。由图4可知,吸附过程与解吸过程中的试验值与模型的预测值几乎分布在y=x直线上,通过R2值可知,Peleg模型拟合效果较好(吸附与解吸过程的R2分别为0.997 6、0.989 1)。说明在温度为25~45 ℃,aw为0.111 6~0.843 4时,使用Peleg数学模型预测罗非鱼片干制品的吸附含水率和解吸含水率较好。

图4 罗非鱼片干制品吸附和解吸平衡含水率试验值与预测值比较
Fig.4 Comparison of test value and predicted value of adsorption and desorption equilibrium moisture of dried tilapia fillets
2.3 罗非鱼片干制品安全贮藏含水率
通过Peleg最佳数学模型可求出,在吸附过程中温度为25、35、45 ℃时,aw=0.60时,绝对安全含水率分别为16.30%、13.68%、13.64%,aw=0.70时,相对安全含水率分别为22.89%、19.21%、19.77%。
根据不同温度条件的Peleg最佳数学模型可确定aw=0.111 6~0.843 4时的平衡含水率,并通过公式(1)求出一定平衡含水率所对应的净等量吸附热和解吸热,绘制净等量吸附热和解吸热与平衡含水率的关系如图5所示。从图5可见:在解吸和吸附过程中,qst与平衡含水率呈负相关性,其曲线呈指数递减;由净等量解吸热曲线可知,物料处于低含水率阶段时,qst值较大,表明物料在干燥后期罗非鱼片中的水分与非水成分相互作用力强,导致干燥速率较慢,干燥时间较长;随着平衡含水率的增加,qst值不断减少,平衡含水率较高时水分与吸附基质表面的结合位点减少,表明物料在干燥前期和中期干燥速率较快,外部环境提供较小的能量就可移除罗非鱼片内部水分。
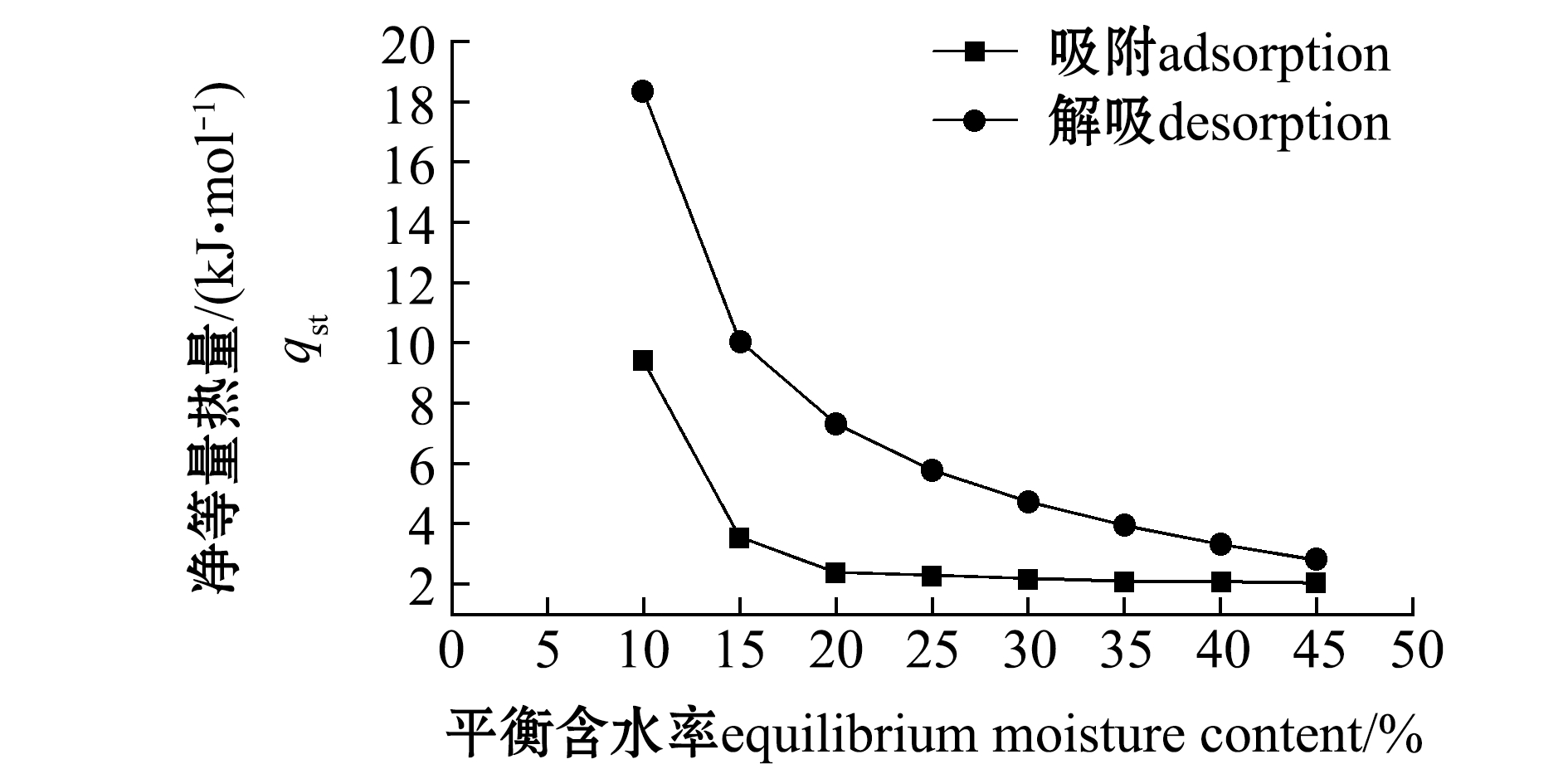
图5 净等量吸附热与解吸热随平衡含水率的变化
Fig.5 Change in the net adsorption heat and the net desorption heat and equilibrium moisture
2.4 微分熵
将净等量吸附热和解吸热值代入公式(2)可求出不同平衡含水率的微分熵,两者的关系如图6所示。从图6可知,随着平衡含水率的增加,微分熵呈现指数递减趋势。原因可能是,当物料含水率较低时,物料表面具有较多的活性位点,物料在环境中表现出较强的吸湿能力,随着含水率的增加,部分活性位点被水分吸附,物料表面的活性位点下降,物料吸湿能力下降,故微分熵值下降。因此,根据微分熵值大小可判断物料的吸湿力,该结论能为不同含水率物料贮藏条件的设置提供理论依据。
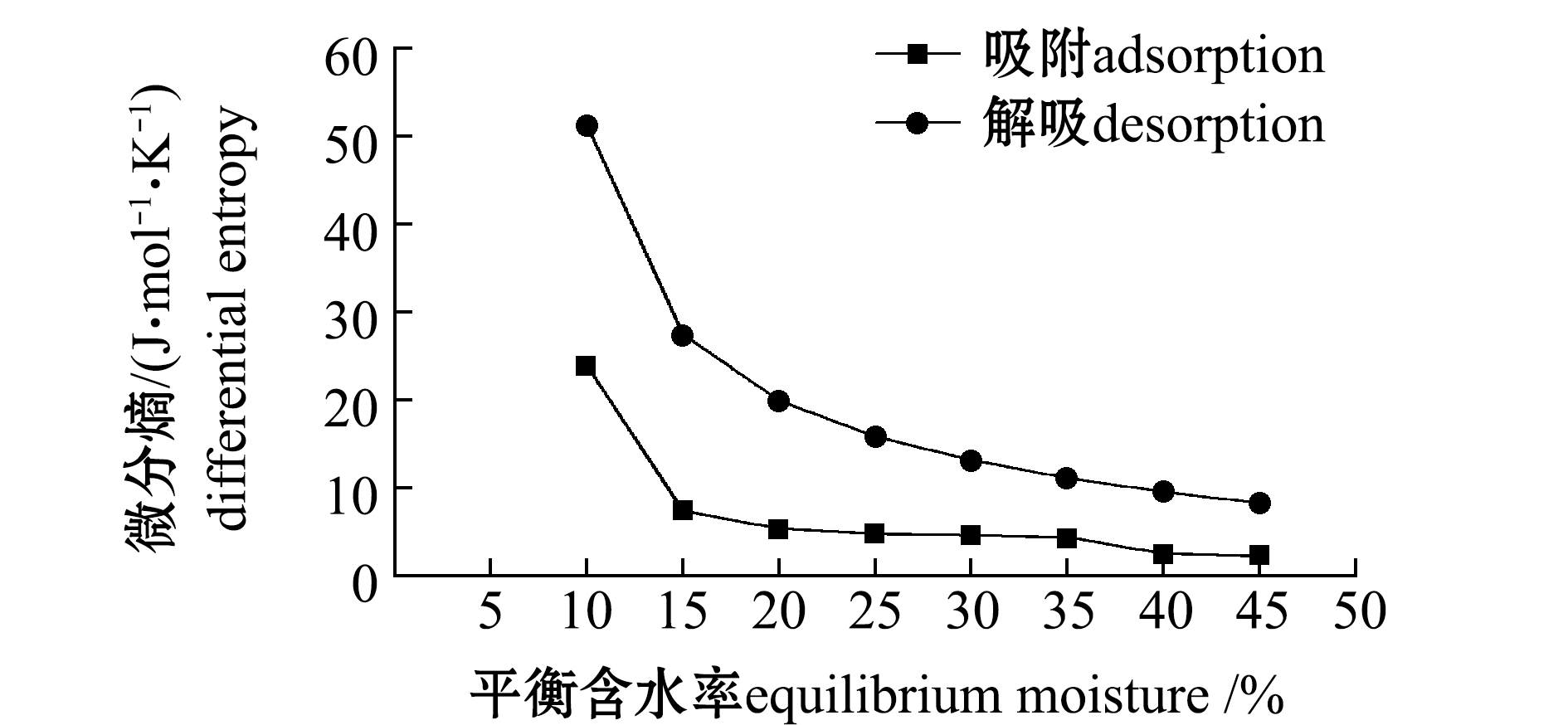
图6 微分熵随平衡含水率的变化
Fig.6 Change of the differential entropy with equilibrium moisture
2.5 焓-熵互补理论
分别对吸附过程中的净等量吸附热与微分熵、解吸过程中的净等量解吸热与微分熵进行线性回归分析,结果如图7所示。从图7可见:解吸-吸附过程中的净等量热量和微分熵存在一定的线性关系;吸附过程中的Tβ=355.39 K,解吸过程中的Tβ=359.54 K,根据公式(4)可求出吸附与解吸的Thm=308.28 K,故Tβ>Thm,表明吸附与解吸过程为焓驱动。此外,通过图7可知,吸附与解吸过程的ΔGβ分别为0.818 4、0.004 kJ/mol,其值均大于零,由此可知,罗非鱼片干制品的解吸过程和吸附过程均为非自发过程。
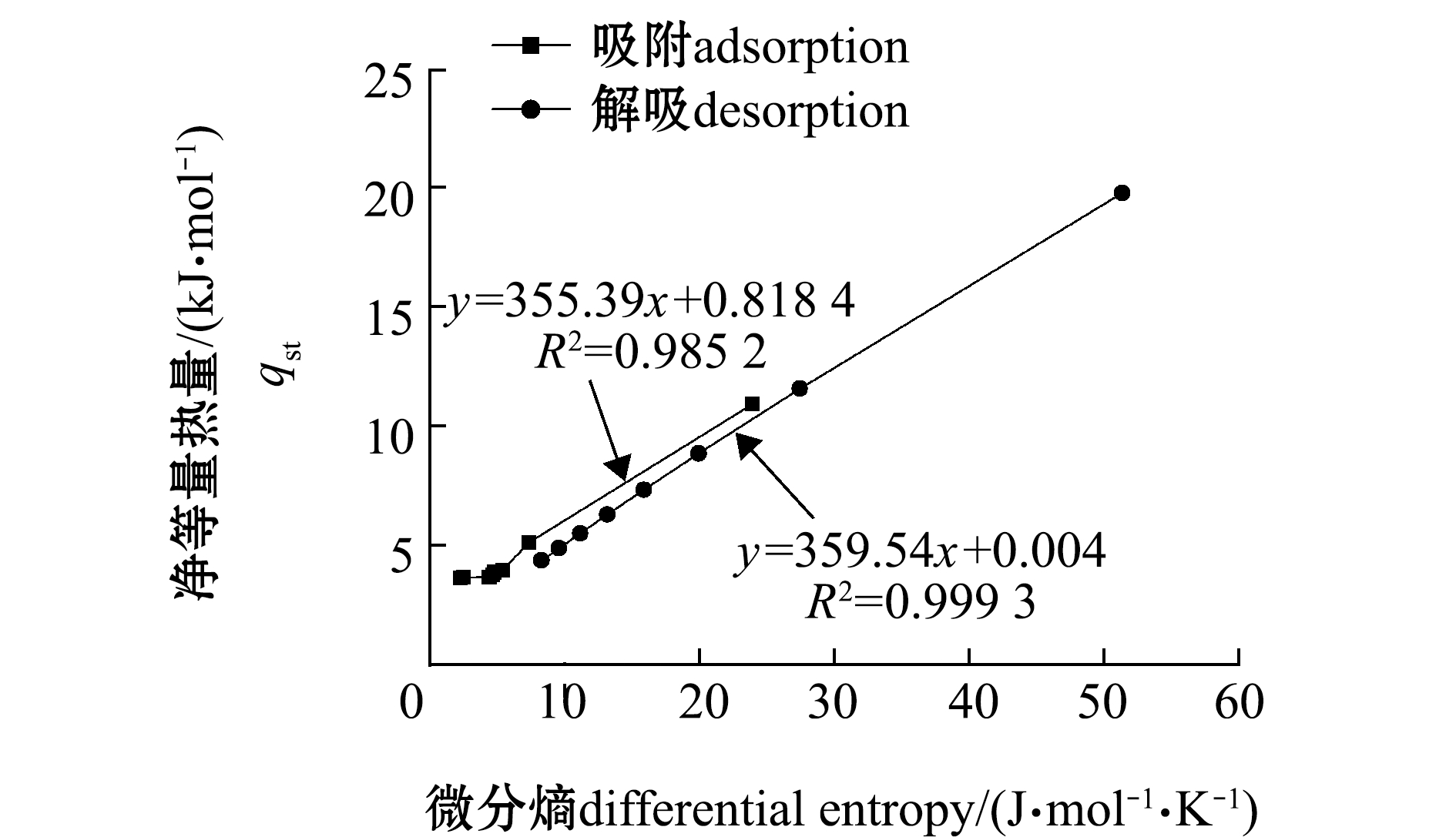
图7 净等量吸附热和解吸热与微分熵之间的关系
Fig.7 Relationship between net adsorption heat and desorption heat and differential entropy
3 讨论
3.1 不同贮藏温度对干制罗非鱼片解吸-吸附等温线的影响
本研究表明,在相同水分活度条件下,干制罗非鱼片解吸-吸附等温线随温度增加呈现下降趋势,但35、45 ℃的解吸-吸附等温线无明显差异;当贮藏温度固定时,罗非鱼片干制品的平衡含水率随水分活度增加呈不断上升趋势,由此可知,贮藏环境湿度对罗非鱼片干制品平衡含水率影响较大。这与龙眼[9]和荔枝[27]的吸附等温线研究结果相似,在不同温度条件下,干制品的解吸-吸附等温线均呈Ⅲ型,而本研究中采用干制罗非鱼片作为试验原料,这表明尽管水产品与水果组织结构不同,但干制品的解吸-吸附等温线确存在相似性。通过干制罗非鱼片解吸-吸附等温线的变化规律可知,干制品在25~35 ℃贮藏时应严格控制环境湿度,从而延长干制品的货架期。
本研究中在一定温度条件下,相同水分活度对应的解吸平衡含水率大于吸附平衡含水率,说明罗非鱼片干制品在解吸和吸附过程存在滞后现象,产生该现象与解吸和吸附过程中的热动力学有关,一般认为是由于解吸和吸附过程中热动力学发生的不可逆过程造成的[28]。当罗非鱼片干制品被置于相对湿度较高的环境中时,吸附在罗非鱼片干制品内的水分未完全到达极性位点;在解吸过程中,随着水分的逸出物料不断收缩,束缚水逐渐接近极性位点并保持平衡,从而导致物料对水分的束缚力下降,由此产生滞后现象。
3.2 平衡含水率对罗非鱼片干制品热力学性质的影响
本研究表明,净等量解吸热和吸附热曲线均随平衡含水率的增加呈现不断下降趋势,最终趋于平衡,出现该现象是由于平衡含水率增加导致基质表面的结合位点不断减少所造成的。张雪峰等[29]研究不同温度条件下甘蓝型油菜籽的净等量解吸热和吸附热曲线,以及郑龙金等[30]研究不同温度条件下黄芩的净等量解吸热和吸附热变化曲线,也均出现随平衡含水率的增加呈现不断下降趋势现象。了解物料的解吸等温线变化趋势有利于优化工艺条件,本研究中通过净等量解吸热和吸附热曲线可知,物料在干燥初期其内部水分含量较高,只需少量能量便可除去物料表层水分,但当物料内部平衡含水率小于20%以下时,则需要更多能量去除物料内部水分。如果继续干燥,物料表面出现硬化现象,水分扩散受阻,干燥速率下降[1]。此时应对物料采用间歇方式进行干燥,使物料内部水分有充足时间迁移到表面[31],以防止物料表面硬化,有利于提高干制品质量并缩短干燥时间。本研究中采用的温度范围只有25~35 ℃,后期应进一步研究更高温度范围内干制品的净等量解吸热和吸附热曲线与平衡含水率的变化关系。
4 结论
1)基于真空冷冻-热泵联合干制罗非鱼片的水分解吸-吸附等温线呈Ⅲ型,在25~45 ℃和aw=0.111 6~0.843 4范围内,Peleg数学模型是描述基于真空冷冻-热泵联合干制罗非鱼片的解吸-吸附等温线的最佳模型。通过不同温度对应的最佳吸附等温线方程算出25、35、45 ℃时罗非鱼片干制品的绝对安全含水率分别为16.30%、13.68%、13.64%,相对安全含水率分别为22.89%、19.21%、19.77%。说明在一定温度和水分活度范围内,可通过Peleg数学模型能较好地预测出罗非鱼片干制品的绝对安全和相对安全含水率,有利于罗非鱼片干制品的贮藏。
2)净等量吸附热、解吸热及微分熵同步分析表明,解吸-吸附等温线的净等量吸附热、解吸热和微分熵均随平衡含水率的增加呈现递减趋势;熵-焓互补理论分析表明,干制罗非鱼片的解吸-吸附过程均为焓驱动,且均属于非自发性。通过微分熵与等温吸附热、解吸附热之间的线性关系可为罗非鱼片的贮藏与干燥提供一定的理论依据。
[1] LUO J,LI M,ZHANG Y,et al.The low-field NMR studies the change in cellular water in tilapia fillet tissue during different drying conditions[J].Food Science & Nutrition,2021,9(5):2644-2657.
[2] BAHLOUL N,BOUDHRIOUA N,KECHAOU N.Moisture desorption-adsorption isotherms and isosteric heats of sorption of Tunisian olive leaves (Olea europaea L.)[J].Industrial Crops and Products,2008,28(2):162-176.
[3] MENKOV N D,DINKOV K T.Moisture sorption isotherms of tobacco seeds at three temperatures[J].Journal of Agricultural Engineering Research,1999,74(3):261-266.
[4] SINIJA V R,MISHRA H N.Moisture sorption isotherms and heat of sorption of instant (soluble) green tea powder and green tea granules[J].Journal of Food Engineering,2008,86(4):494-500.
[5] YAZDANI M,SAZANDEHCHI P,AZIZI M,et al.Moisture sorption isotherms and isosteric heat for pistachio[J].European Food Research and Technology,2006,223(5):577-584.
[6] AGHA M K K,LEE W S,BUCKLIN R A,et al.Sorption isotherms for triticale seed[J].Transactions of the Asabe,2014,57(3):901-904.
[7] BARATI M,ZARE D,ZOMORODIAN A.Moisture sorption isotherms and thermodynamic properties of safflower seed using empirical and neural network models[J].Journal of Food Measurement and Characterization,2016,10(2):236-246.
[8] LIN G Y,YANG H P,WANG X H,et al.The moisture sorption characteristics and modelling of agricultural biomass[J].Biosystems Engineering,2016,150:191-200.
[9] 马兴灶,连海山,吕莹,等.干制“储良”龙眼吸附等温线与热力学特性研究[J].食品与发酵工业,2019,45(19):98-103.
MA X Z,LIAN H S,LÜ Y,et al.Adsorption isotherms and thermodynamic characteristics of dried “Chuliang” longyan[J].Food and Fermentation Industries,2019,45(19):98-103.(in Chinese)
[10] ROMAN-GUTIERREZ A D,GUILBERT S,CUQ B.Distribution of water between wheat flour components:a dynamic water vapour adsorption study[J].Journal of Cereal Science,2002,36(3):347-355.
[11] MAJD K M,KARPARVARFARD S H,FARAHNAKY A,et al.Thermodynamic properties of water sorption isotherms of grape seed[J].International Agrophysics,2014,28:63-71.
[12] PONWIBOON N,ROJANAKORN T.Desorption isotherms and drying characteristics of Nile tilapia fish sheet[J].International Food Research Journal,2017,24(3):1292-1300.
[13] 关志强,王秀芝,李敏,等.罗非鱼肉干燥过程平衡含水率模型研究[J].食品科学,2012,33(15):118-121.
GUAN Z Q,WANG X Z,LI M,et al.Modeling of equilibrium moisture content of tilapia fillets during drying process[J].Food Science,2012,33(15):118-121.(in Chinese)
[14] 段振华,张玲,汪菊兰,等.罗非鱼鱼肉的解吸平衡规律研究[J].食品科学,2011,32(增刊1):82-85.
DUAN Z H,ZHANG L,WANG J L,et al.Study on characteristic of isothermal desorption of tilapia meats[J].Food Science,2011,32(sup 1):82-85.(in Chinese)
[15] 罗静,李敏,关志强.干燥工艺对罗非鱼片品质的影响[J].南方农业学报,2020,51(7):1764-1775.
LUO J,LI M,GUAN Z Q.Effects of drying processes on quality of tilapia fillets[J].Journal of Southern Agriculture,2020,51(7):1764-1775.(in Chinese)
[16] 朱文学.食品干燥原理与技术[M].北京:科学出版社,2009.
ZHU W X.Principle and technology of food drying[M].Beijing: Science Press,2009.(in Chinese)
[17] 郝光宗,邢丽缘,梁强威.饱和盐水溶液湿度固定点:(2)-数据来源与盐溶液选择[J].传感器世界,1999(12):10-14.
HAO G Z,XING L Y,LIANG Q W.Moisture fixation points for saturated brine solutions:(2)-data source and salt solution selection[J].Sensor World,1999(12):10-14.(in Chinese)
[18] 万云雷,韩红霞,高梦祥.稻谷吸附特性及安全水分研究[J].食品科技,2015,40(12):124-127.
WAN Y L,HAN H X,GAO M X.Moisture adsorption characteristics and safe moisture of rice[J].Food Science and Technology,2015,40(12):124-127.(in Chinese)
[19] ARGYROPOULOS D,ALEX R,KOHLER R,et al.Moisture sorption isotherms and isosteric heat of sorption of leaves and stems of lemon balm (Melissa officinalis L.) established by dynamic vapor sorption[J].Food Science and Technology,2012,47(2):324-331.
[20] BEJAR A K,MIHOUBI N B,KECHAOU N.Moisture sorption isotherms-experimental and mathematical investigations of orange (Citrus sinensis) peel and leaves[J].Food Chemistry,2012,132(4):1728-1735.
[21] HERAS R M L,HEREDIA A,CASTELL M L,et al.Moisture sorption isotherms and isosteric heat of sorption of dry persimmon leaves[J].Food Bioscience,2014,7:88-94.
M L,et al.Moisture sorption isotherms and isosteric heat of sorption of dry persimmon leaves[J].Food Bioscience,2014,7:88-94.
[22] TSAMI E.Net isosteric heat of sorption in dried fruits[J].Journal of Food Engineering,1991,14(4):327-335.
![]() B,BE
B,BE E A V,KAYA M,et al.Moisture adsorption isotherms and thermodynamics properties of sucuk (Turkish dry-fermented sausage)[J].Food and Bioproducts Processing,2011,89(4):449-456.
E A V,KAYA M,et al.Moisture adsorption isotherms and thermodynamics properties of sucuk (Turkish dry-fermented sausage)[J].Food and Bioproducts Processing,2011,89(4):449-456.
[24] MCMINN W,AL-MUHTASEB A H,MAGEE T R A.Enthalpy-entropy compensation in sorption phenomena of starch materials[J].Food Research International,2005,38(5):505-510.
[25] KRUG R R,HUNTER W G,GRIEGER R A.Enthalpy-entropy compensation.1.some fundamental statistical problems associated with the analysis of van’t Hoff and Arrhenius data[J].The Journal of Physical Chemistry,1976,80(21):2335-2341.
[26] LAHSASNI S,KOUHILA M,MAHROUZ M,et al.Experimental study and modelling of adsorption and desorption isotherms of prickly pear peel (Opuntia ficus indica)[J].Journal of Food Engineering,2002,55(3):201-207.
[27] 李辉,林河通,林毅雄,等.干制荔枝果肉吸附等温线及热力学性质[J].农业工程学报,2014,30(22):309-315.
LI H,LIN H T,LIN Y X,et al.Moisture sorption isotherms and thermodynamic properties of dried litchi pulp[J].Transactions of the Chinese Society of Agricultural Engineering,2014,30(22):309-315.(in Chinese)
[28] SAMAPUNDO S,DEVLIEGHERE F,DE MEULENAER B,et al.Sorption isotherms and isosteric heats of sorption of whole yellow dent corn[J].Journal of Food Engineering,2007,79(1):168-175.
[29] 张雪峰,黎斌,彭桂兰,等.甘蓝型油菜籽水分解吸等温线及热力学性质[J].中国粮油学报,2019,34(6):59-67.
ZHANG X F,LI B,PANG G L,et al.Desorption isotherms and thermodynamic properties of rapeseed[J].Journal of the Chinese Cereals and Oils Association,2019,34(6):59-67.(in Chinese)
[30] 郑龙金,何雁,张俊鸿,等.黄芩饮片等温吸附与解吸曲线及热力学性质研究[J].中国中药杂志,2016,41(5):830-837.
ZHENG L J,HE Y,ZHANG J H,et al.Isothermal adsorption,desorption and thermodynamic properties of Scutellaria baicalensis pieces[J].China Journal of Chinese Material Medica,2016,41(5):830-837.(in Chinese)
[31] 盘喻颜,段振华,钟静妮.利用低场核磁共振技术分析月柿果片微波间歇干燥过程中的内部水分变化[J].食品工业科技,2021,42(14):33-39.
PAN Y Y,DUAN Z H,ZHONG J N.Analysis of internal moisture changes of persimmon slices during intermittent microwave drying using low-field NMR[J].Science and Technology of Food Industry,2021,42(14):33-39.(in Chinese)