
张磊1、2,王锦旭1,杨贤庆1,魏涯1,杨少玲1
(1.中国水产科学研究院南海水产研究所,农业部水产品加工重点实验室,国家水产品加工技术研发中心,广东 广州 510300;2.上海海洋大学 食品学院,上海 201306)
摘要:为丰富合浦珠母贝Pinctadamartensii的食品种类,制备出酸甜可口、质量安全的合浦珠母贝糖胺聚糖泡腾片,以合浦珠母贝糖胺聚糖为主料,黏合剂、润滑剂、矫味剂和稀释剂为辅料,采用单因素试验和正交试验方法,确定最佳原辅料配比和最优工艺,原辅料经混合、制软材、干燥、整粒、压片等工序制备出泡腾片,并对制备的泡腾片进行质量指标检测和急性经口毒性试验。结果表明:合浦珠母贝糖胺聚糖泡腾片最优配方为(以质量百分比计)糖胺聚糖25%,崩解剂35%(碳酸氢钠与柠檬酸的配比为1∶2),矫味剂三氯蔗糖3%,黏合剂聚乙烯吡咯烷酮(PVP)2%,润滑剂聚乙二醇(PEG)4000 2%,余量为乳糖;按此最优工艺制备的泡腾片直径约为8 mm,重约为200 mg,硬度为5.5~6.5 kg,崩解时间<40 s;急性经口毒性试验表明,14 d观察期内SD大鼠均无异常行为及死亡。研究表明,用本研究优化工艺制得的糖胺聚糖片剂产品表面光滑整洁、口感良好,质量安全,稳定可靠,无毒副作用。
关键词:合浦珠母贝;糖胺聚糖;泡腾片;正交试验;质量分析
泡腾片是含有泡腾崩解剂的片剂,崩解剂一般由酸源和碳源组成,遇水后其中的酸和碱发生化学反应并放出二氧化碳气体,使片剂迅速崩解和融化[1]。泡腾片不仅方便携带、保质期长,而且容易吸收、生物利用度高,特别适合老年人或者有咀嚼困难的人群,起初用于制药领域,近年来在食品和保健品领域也进行了大量研究,且成果显著,越来越受到人们的欢迎,如维生素C泡腾片[2]、黑莓泡腾片[3]等。
合浦珠母贝Pinctadamartensii[4-6]是中国南海珠母贝的主要贝种之一,分布在广东、广西和海南沿海地区,每年珠农采珠后剩余的加工副产物珍珠贝肉高达3500~4000 t,大多为鲜食或粗加工后食用,深加工率较低,保藏期短,价格低廉。合浦珠母贝贝肉除了富含优质蛋白质和多种矿物质外,其中的糖胺聚糖(Glycosaminoglycans,GAGs)作为一种天然的生物活性多糖也越来越引人关注。糖胺聚糖,也称氨基多糖或酸性黏多糖,是由重复的二糖单位构成的长链多糖,存在于多数海洋动物的组织中,具有调节免疫[7]、抗肿瘤[8-9]、降血脂[10]、抗氧化[11]等多种生物活性[12],可用于营养健康食品领域,具有重要的经济开发价值。中国是贝类养殖大国,资源极为丰富,利用加工副产物提取糖胺聚糖,开发出新产品,对实现合浦珠母贝高值化利用和养殖业健康持续发展具有重要意义[13]。本研究中,以合浦珠母贝糖胺聚糖为主料,泡腾崩解剂、黏合剂、润滑剂、矫味剂和稀释剂等为辅料,制备出酸甜可口、质量安全的泡腾片,在补充功能因子的同时,增强适口感,旨在为人类提供一种新型的营养健康食品,促进贝类资源的高值化利用,丰富合浦珠母贝的食品种类。
试验用合浦珠母贝贝肉全脏器购自广东省徐闻县,于冰箱(-18 ℃)中保存,糖胺聚糖精制品从合浦珠母贝贝肉中提取,用1,9-二甲基亚甲基蓝法测得纯度均在80%以上,置于冰箱(-4 ℃)中冷藏备用。
主要试剂:中性蛋白酶(酶活力100 U/mg)、胰蛋白酶(酶活力250 U/mg)、透析袋、DEAE-52纤维素填料均购自广州齐云生物技术有限公司,聚乙二醇(PEG)4000 购自汕头市光华化学厂,聚乙烯吡咯烷酮(PVP)购自美国陶氏化学公司,乳糖购自德国MEGGLE公司,柠檬酸、碳酸氢钠、甘露糖、三氯蔗糖等均为食品级。
主要仪器设备:Milli-Q超纯水机(美国MILLIPORE公司);HWS24电热恒温水浴锅(上海一恒科学仪器有限公司);Alpha1-4冷冻干燥机(德国Christ;Delta320);精密pH计[梅特勒-托利多仪器(上海)有限公司];TDP-1单冲压片机(上海天凡药机制造厂);BJ-3崩解时限测定仪(北京中兴伟业仪器有限公司);78X-3片剂四用测试仪(上海黄海药检仪器厂)。
1.2.1 合浦珠母贝糖胺聚糖提取工艺 将合浦珠母贝全脏器在常温下自然解冻,搅成肉泥备用。取一定量贝肉加2倍体积的水,55 ℃下浸提4 h,4 ℃下浸提12 h;加入中性蛋白酶和胰蛋白酶,pH调至7.6,复合酶解4 h,煮沸10 min灭酶,以10 000 r/min离心20 min,取上清液,重复离心操作直至除去杂质蛋白;上清液pH调至7.0,加70%乙醇4 ℃下醇沉12 h,离心取沉淀,经冷冻干燥得糖胺聚糖粗制品,粗多糖经过透析,用DEAE-52纤维素阴离子柱层析分离得到合浦珠母贝糖胺聚糖精制品[14]。
1.2.2 合浦珠母贝糖胺聚糖泡腾片制备 将合浦珠母贝糖胺聚糖与崩解剂、乳糖按适当比例混合,搅拌均匀后过100目筛,向混合原料缓慢喷洒质量分数为10%的PVP乙醇溶液,同时不断搅拌均匀,制成软硬适中的软材,过16目筛,使软材变成颗粒,将制成的湿颗粒摊放在搪瓷盘中,于65 ℃下烘干至水分含量为0.5%以下,粉碎过20目筛,加入质量分数为2%的润滑剂和3%的矫味剂,用单冲压片机压片,采用紫外线杀菌机进行紫外杀菌,采用双铝包装按10片每板的规格包装[15]。
1.2.3 单因素试验 影响泡腾片成型的主要因素是酸源和碳源种类、酸碱比例和崩解剂用量,本研究中采用单因素试验,以CO2释放量、pH值为考察指标来确定泡腾崩解剂。因泡腾片具有较强的吸湿性,在制备过程中有一定的难度,因此,本试验中选取吸湿性较小的乳糖为稀释剂,辅助一定的黏合剂和润滑剂提高制粒效果,改善压片进程[16]。采用单因素试验法对处方中各影响因素的作用进行考察,优化制备工艺。
1.2.4 正交试验 通过单因素试验,选出影响泡腾片品质的3个主要因素为崩解剂、黏合剂和润滑剂。为进一步优化糖胺聚糖泡腾片的配方,采用L9(34)正交试验,以崩解时限和硬度为考察指标,优化崩解剂、PVP、PEG4000的添加量。
1.2.5 质量指标的测定方法 采用仪器法测定pH值、硬度、崩解时限;根据GB 5009.3—2016《食品中水分的测定》测定水分含量;采用1,9-二甲基亚甲基蓝法测定糖胺聚糖含量;分别采用BCA试剂盒法、苯酚-硫酸法测定蛋白质和总糖含量;采用湿法消解ICP-MS测定重金属污染物含量;根据GB 4789.2—2010《食品微生物学检验菌落总数测定》、GB 4789.3—2010《食品微生物学检验大肠菌群计数》等测定微生物指标;根据中国药典2015年版测定重量差异;采用失重法测定CO2释放量[17];采用固定漏斗法测定休止角[18]。
1.2.6 合浦珠母贝糖胺聚糖咀嚼片的SD大鼠急性经口毒性试验 SD大鼠为SPF级,雌、雄各半,体质量为180~200 g,购自广东省医学动物实验中心[动物生产许可证号SCXK(粤)2013-0003,试验动物质量合格证明号44007200037911]。动物饲养于广东省医学动物试验中心SPF级动物试验设施[许可证号SYXK(粤)2013-0002,动物试验证明号00165703]中,试验相关的内容和程序遵从试验动物使用和管理的相关法律法规及试验动物伦理委员会的相关规定。
将雌、雄各20只SD大鼠随机分为溶剂对照组和合浦珠母贝糖胺聚糖泡腾片组,每组20只,雌、雄各10只,采用最大耐受量试验法进行试验,按大鼠最大灌胃容量20 mL/kg(体质量),24 h内灌胃3次,两次灌胃时间间隔4~6 h。以蒸馏水为溶剂对照组,合浦珠母贝糖胺聚糖泡腾片作为受试物,加蒸馏水溶解,剂量为90 g/kg(体质量),其中的功能因子糖胺聚糖剂量为22.5 g/kg(体质量)。观察并记录给予受试物过程和观察期内动物的中毒和死亡情况,观察期为14 d,观察期内中毒死亡以及观察期满处死的动物均应解剖,肉眼观察,如发现组织或脏器出现异常,进一步作组织病理学检查,分别在第0、1、3、7、14天称重,急性毒性剂量分级表对受试物的毒性评价规定如表1所示[19]。
表1急性经口毒性的评价规定
Tab.1Evaluationregulationsofacuteoraltoxicity

LD50/(mg·kg-1)毒性分级toxicity grading<1极毒1~50剧毒51~500中等毒501~5000低毒5001~15000实际无毒>15000无毒
试验数据以平均值±标准差(mean±S.D.)表示,采用SPSS 22.0软件进行统计分析,使用正交设计助手II专业版对试验数据进行处理。
2.1.1 崩解剂酸源选择 由化学反应原理可知,碳酸氢钠、碳酸钠产气效果不同,产气量相同时碳酸氢钠用量更少,因此,选用碳酸氢钠为崩解剂碳源。以碳酸氢钠作为崩解剂碳源,对比相同添加量的柠檬酸、富马酸、酒石酸对泡腾片品质的影响,结果见表2。由表2可知,由柠檬酸作为崩解剂酸源的泡腾片外观良好,溶解后无可见不溶物,且口感较好。因此,选择柠檬酸作为酸源。
表2不同酸源对糖胺聚糖泡腾片品质的影响
Tab.2Effectsofdifferentacidsourcesonqualityoftheglycosaminoglycaneffervescenttablets
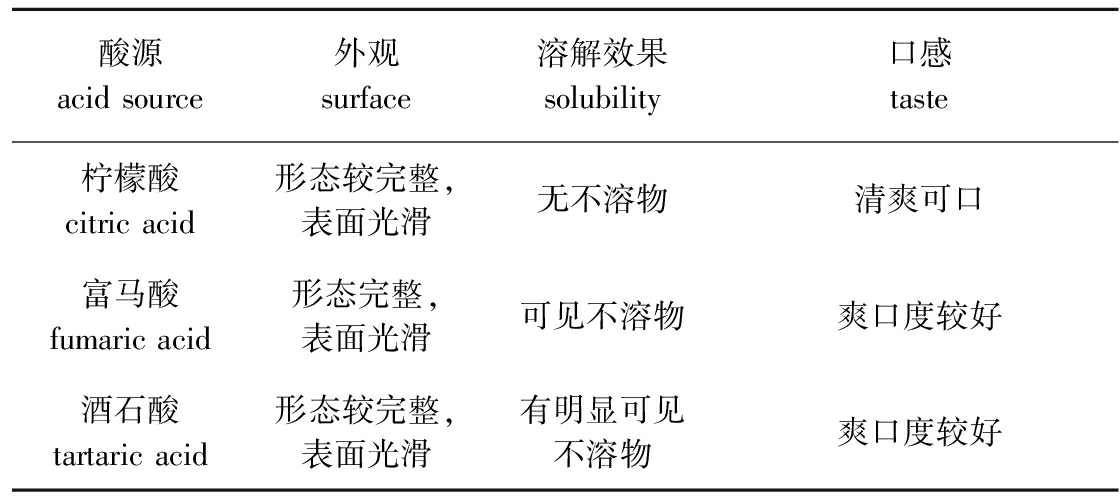
酸源acid source外观surface溶解效果solubility口感taste柠檬酸citric acid形态较完整,表面光滑无不溶物清爽可口富马酸fumaric acid形态完整,表面光滑可见不溶物爽口度较好酒石酸tartaric acid形态较完整,表面光滑有明显可见不溶物爽口度较好
2.1.2 崩解剂配比的确定 选用碳酸氢钠和柠檬酸为崩解剂,通过调整碳酸氢钠与柠檬酸的用量改善泡腾片的品质。按照基础配方[20],糖胺聚糖25%,碳酸氢钠和柠檬酸40%,黏合剂2%,矫味剂3%,乳糖为填充剂,以泡腾片CO2释放量和pH值为指标,考察碳酸氢钠和柠檬酸的比例,其中碳酸氢钠与柠檬酸的质量比分别为3∶1、2∶1、1∶1、1∶2、1∶3,试验结果见表3。由表3可知,随着碳酸氢钠比例的增加,CO2释放量也显著增加(P<0.05),当二者的比例大于1∶1时,CO2释放量增加缓慢,溶液pH也逐渐升高至接近中性。在考虑CO2释放量的同时,还要兼顾酸碱反应后产生的柠檬酸钠,如生成量过多会有不愉快的涩味,故碳酸氢钠的用量不宜过高。当碳酸氢钠和柠檬酸的比例为1∶2时,CO2释放量较多,且pH符合要求,口感较好,因此,选用碳酸氢钠与柠檬酸比例为1∶2。
表3崩解剂配比对糖胺聚糖泡腾片CO2释放量和反应溶液pH的影响
Tab.3EffectsofdisintegrantratioonCO2amountandpHofglycosaminoglycaneffervescenttablets
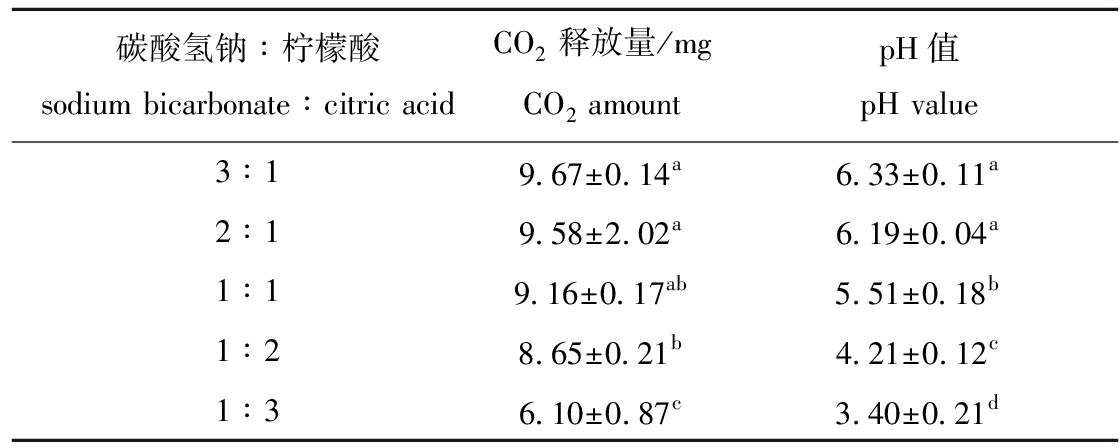
碳酸氢钠∶柠檬酸sodium bicarbonate∶citric acidCO2释放量/mgCO2 amountpH值pH value3∶19.67±0.14a6.33±0.11a2∶19.58±2.02a6.19±0.04a1∶19.16±0.17ab5.51±0.18b1∶28.65±0.21b4.21±0.12c1∶36.10±0.87c3.40±0.21d
注:同列中标有不同小写字母者表示组间有显著性差异(P<0.05),标有相同小写字母者表示组间无显著性差异(P>0.05),下同
Note:The means with different letters within the same column are significantly different in the groups at the 0.05 probability level, and the means with the same letters within the same column are not significant differences, et sequentia
2.1.3 崩解剂添加量的确定 崩解剂酸碱反应产生的柠檬酸钠为偏碱性的盐,当泡腾片中碳酸氢钠与柠檬酸添加量适当时,才能使泡腾片有良好CO2释放量和口感,同时崩解剂的添加量还会对崩解时限产生重要影响[21]。本试验中以崩解时限和CO2释放量为指标,考察泡腾片崩解剂添加量,试验结果见表4。由表4可知,随着泡腾崩解剂用量的增加,其崩解时限呈先减小后增加的趋势,可能是因为添加量增加,辅料比例减少,不能迅速分散。当添加量为35%时,其崩解时限最小,其次是添加量为30%,当添加量为25%时,崩解时限最长;在CO2释放量方面,当添加量大于35%时,均符合要求。综上所述,可以选用35%作为崩解剂的添加量,即碳酸氢钠为11.6%,柠檬酸为23.2%。
表4泡腾崩解剂添加量对糖胺聚糖泡腾片崩解时限和发泡量的影响
Tab.4EffectsoftheeffervescentdisintegrantamountonthedisintegrationtimeandCO2amount
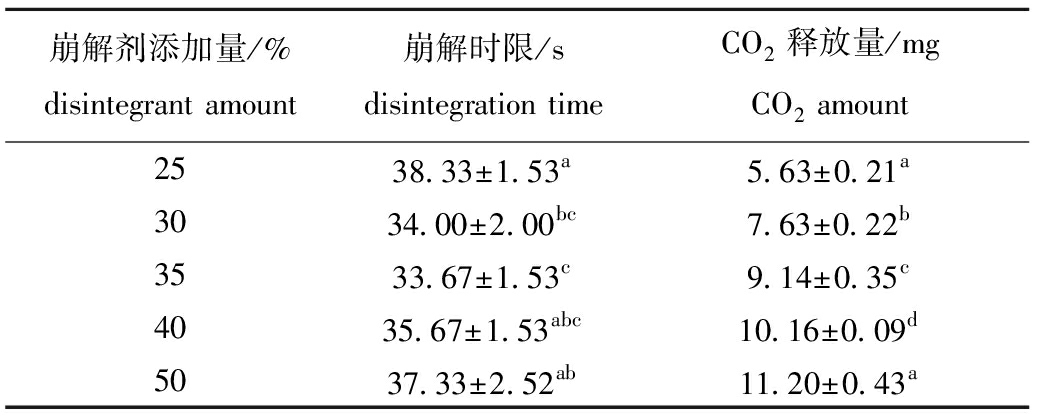
崩解剂添加量/%disintegrant amount崩解时限/sdisintegration timeCO2释放量/mgCO2 amount2538.33±1.53a5.63±0.21a3034.00±2.00bc7.63±0.22b3533.67±1.53c9.14±0.35c4035.67±1.53abc10.16±0.09d5037.33±2.52ab11.20±0.43a
2.1.4 黏合剂添加量的确定 聚乙烯吡咯烷酮(PVP)、羟丙基甲基纤维素(HPMC)等均为亲水性的黏合剂,制成的颗粒表面具有亲水性,水分易湿润、透入,加快片剂崩解速度。本试验中采用酸碱混合制粒工艺,需严格控制接触水分,所以选择可溶于无水乙醇的PVP作为黏合剂。以崩解时限和片剂硬度为评价指标,分别考察质量分数为0%、2%、4%、6%、8%的PVP乙醇溶液对糖胺聚糖泡腾片质量指标的影响,结果见表5。由表5可知:当PVP添加量大于2%时,泡腾片崩解时限显著增加(P<0.05),硬度也随之增大,不易崩解,容易出现裂片现象,且所制软材偏黏,颗粒不均匀,压片易黏冲;当PVP添加量小于2%时,制得软材较松散,颗粒粉末增多,压片硬度偏小,泡腾片易松散;当PVP添加量为2%时,黏性好,干颗粒经过手捻能粉碎成有粗糙感的细粉,且崩解时限和硬度适宜。因此,选择2% PVP作为最佳黏合剂添加量。
表5PVP添加量对泡腾片崩解时限和硬度的影响
Tab.5EffectsofPVPamountonthedisintegrationtimeandhardnessofeffervescenttablets
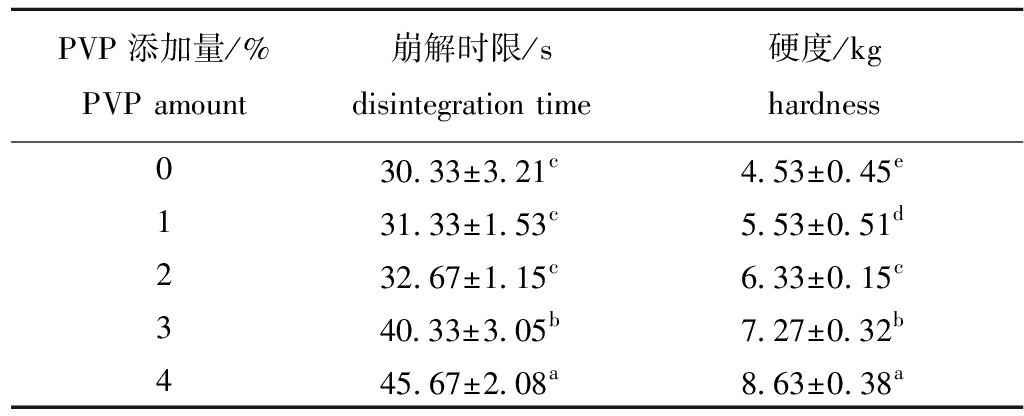
PVP添加量/%PVP amount 崩解时限/sdisintegration time硬度/kghardness030.33±3.21c4.53±0.45e131.33±1.53c5.53±0.51d232.67±1.15c6.33±0.15c340.33±3.05b7.27±0.32b445.67±2.08a8.63±0.38a
2.1.5 润滑剂添加量的确定 为避免制片时由于颗粒流动性不佳,出现片重波动大、出片困难、光洁度低等现象,颗粒在压片前要加入润滑剂。常用的片剂润滑剂有硬脂酸镁、滑石粉、十二烷硫酸钠(SDS)、聚乙二醇(PEG)4000等,其中,硬脂酸镁、滑石粉为水不溶性,泡腾片在水中崩解后,会在水表面形成一层浑浊的薄膜,影响产品的感官品质;SDS作为表面活性剂,可减小水表面活性,在泡腾片崩解后会残留大量气泡,影响泡腾片所产生的二氧化碳排放和溶剂可观性;水溶性润滑剂PEG4000对泡腾片崩解后的澄清度无影响,且润滑性和抗黏性较好,宜选用[22-23]。
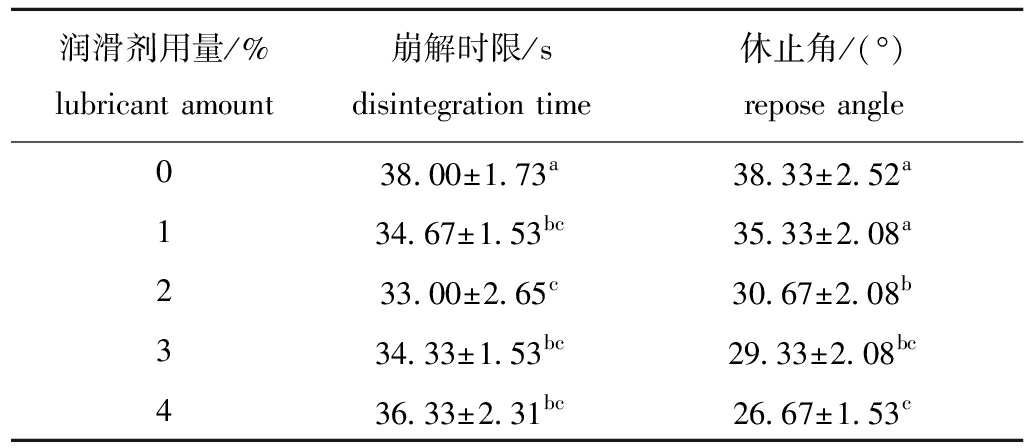
本试验中选择质量分数为0%、1%、2%、3%、4%的PEG4000,以休止角和硬度为评定指标,筛选最适的润滑剂添加量,试验结果见表6。润滑剂可使泡腾片的密度更加均匀,降低颗粒与压片机孔壁间摩擦力。由表6可知:添加不同质量分数的润滑剂对崩解时限、休止角有不同程度的影响,当润滑剂添加量小于2%时,休止角显著增大(P<0.05),颗粒流动性差,出现黏冲现象;当润滑剂加入过多时,崩解时限延长, 可能是因为过多的润滑剂阻碍了水分进入片剂中心,降低酸碱的反应速度;当润滑剂添加量为2%时,能在压片中有效地改善颗粒或粉末的流动性,所得片剂的崩解时限较好,无黏冲现象。因此,确定润滑剂添加量为2%。
表6润滑剂添加量对泡腾片崩解时限和休止角的影响
Tab.6Effectsoflubricantamountonthedisintegrationtimeandthereposeangleofeffervescenttablets
2.1.6 矫味剂添加量的确定 蔗糖、阿斯巴甜、三氯蔗糖是食品中常用的矫味剂,甜度较高的阿斯巴甜或三氯蔗糖,可使泡腾片的崩解时限不受矫味剂添加量的影响,亦可避免糖含量高导致的吸潮结块现象。由预试验发现,阿斯巴甜较三氯蔗糖溶解度小、崩解时间长,而三氯蔗糖极易溶于水,甜味更容易被接受,因此,选用三氯蔗糖作为矫味剂。三氯蔗糖是以蔗糖为原料的功能性甜味剂,无热量,不会引起血糖增加,安全性高,口感纯正,甜度为蔗糖的600倍,考察三氯蔗糖添加量分别为1%、2%、3%、4%、5%时对泡腾片口感的影响,结果见表7。从表7可知,当三氯蔗糖添加量为3%时,甜度适中。同时为了解决糖胺聚糖药物剂量小难以压片,并具有一定黏性易黏结成团的问题,可复配一定量的乳糖和甘露糖作为泡腾片的稀释剂和矫味剂,既能增加片剂的质量,还可分散主料,减少主料成分剂量偏差。
表7三氯蔗糖添加量对泡腾片口感的影响
Tab.7Effectsofsucraloseamountonthetasteofeffervescenttablets

三氯蔗糖用量sucralose amount/%甜味分析 sweetness analysis1甜味很淡2甜味一般3甜度适中4较甜5很甜
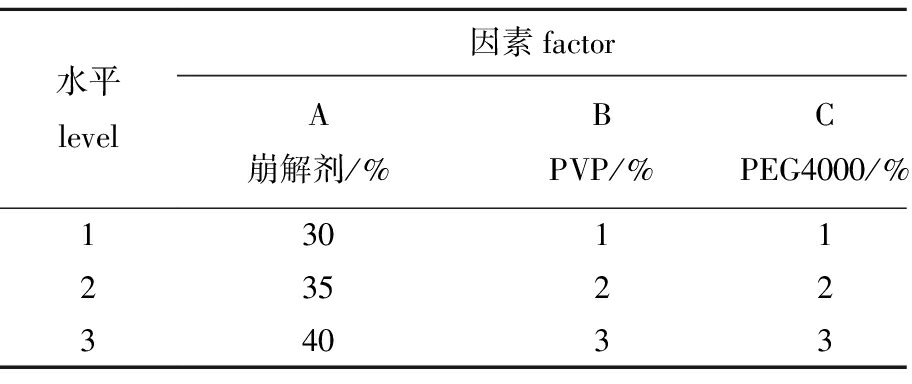
采用L9(34)正交试验表设计试验,以崩解剂(A)、黏合剂(B)和润滑剂(C)的添加量为考察因素,以崩解时限和硬度为评价指标,试验因素水平及正交试验结果见表8、9,方差分析结果见表10、表11。
表8正交试验因素水平表
Tab.8Factorsandlevelsoforthogonalexperiments
水平level因素factorA崩解剂/%BPVP/%CPEG4000/%130112352234033
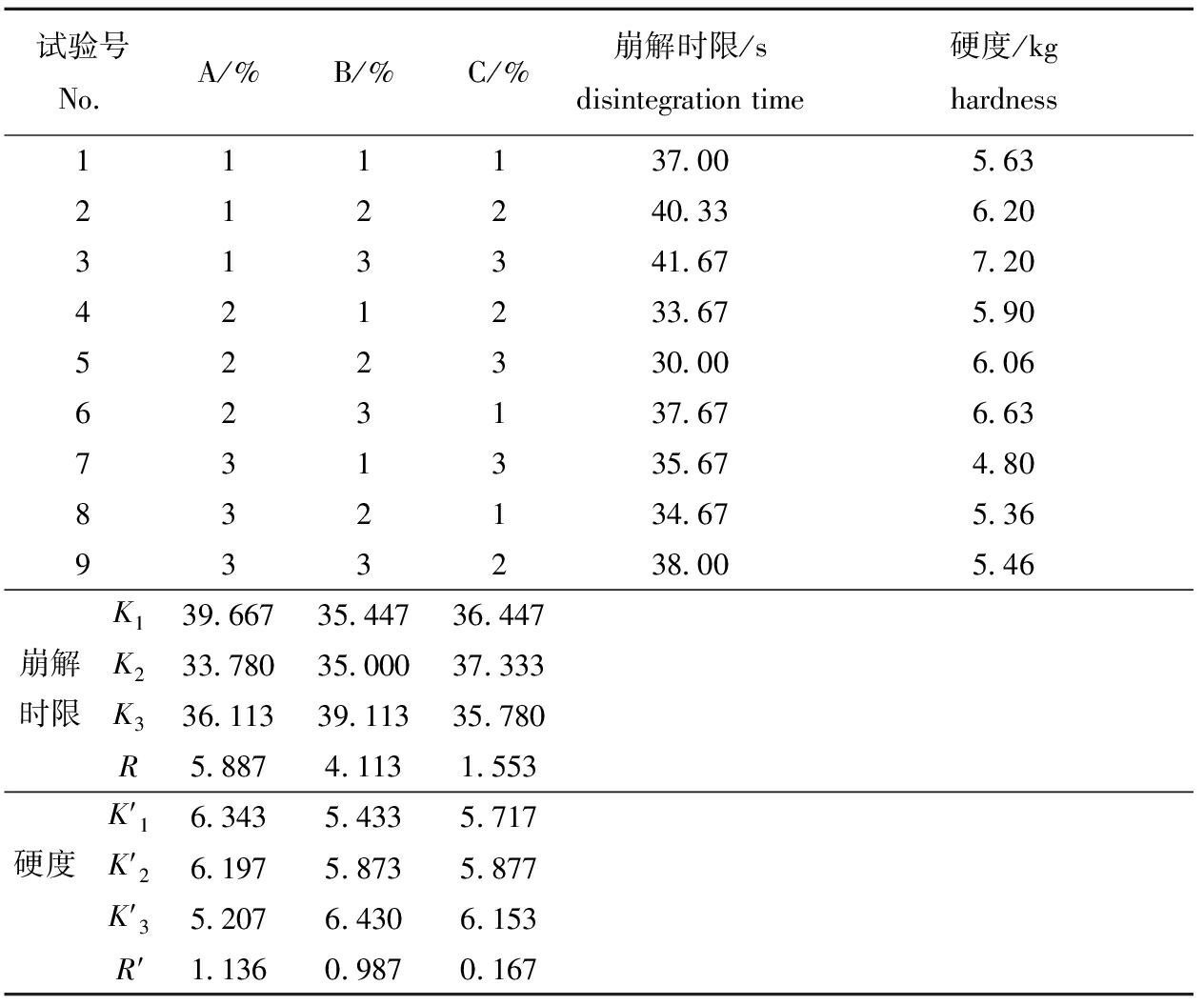
表9正交试验设计及结果
Tab.9Designandresultsoforthogonaltests
试验号No.A/%B/%C/%崩解时限/sdisintegration time硬度/kghardness111137.005.63212240.336.20313341.677.20421233.675.90522330.006.06623137.676.63731335.674.80832134.675.36933238.005.46 K139.66735.44736.447崩解 K233.78035.00037.333时限 K336.11339.11335.780 R5.8874.1131.553 K′16.3435.4335.717硬度 K′26.1975.8735.877 K′35.2076.4306.153 R′1.1360.9870.167
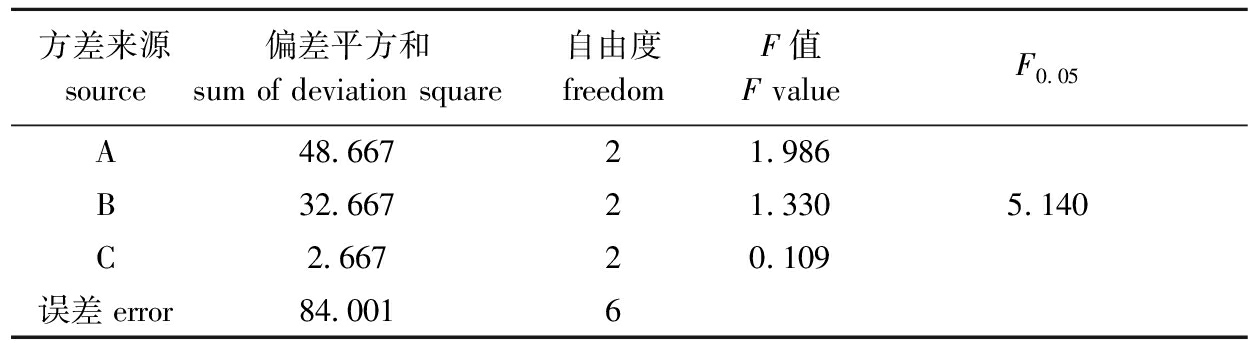
表10崩解时限方差分析结果
Tab.10Analysisofvariancefordisintegrationtime
方差来源source偏差平方和sum of deviation square自由度freedomF值F valueF0.05A48.66721.986B32.66721.3305.140C2.66720.109误差error84.0016
表11硬度方差分析结果
Tab.11Analysisofvarianceforhardness

方差来源source偏差平方和residual sum of square自由度freedomF值F valueF0.05A2.29422.235B1.46821.4305.140C0.05020.049误差error3.8126
由极差分析可以看出,3个因素对崩解时限和硬度影响的大小顺序均为A>B>C,即崩解剂添加量的影响最大,黏合剂添加量的影响次之,润滑剂添加量的影响最小,崩解时限正交试验的最优组合为A1B3C2,硬度正交试验的最优组合为A1B3C3,即崩解剂添加量为35%、黏合剂添加量2%时,润滑剂添加量为2%或3%时,崩解时限和硬度指标均较好。方差分析结果显示,3个因素对崩解时限、硬度的影响均不显著(P>0.05)。根据前期糖胺聚糖活性评价试验结果和成人—小鼠剂量换算公式,合浦珠母贝糖胺聚糖的小鼠起效剂量为0.25 mg/d,按照公式换算为成人起效剂量为200 mg/d,按照每天服用四片咀嚼片计算,每片中的糖胺聚糖添加量为25%[24]。综合考虑,最终确定泡腾片各组分最佳配比为糖胺聚糖25%、崩解剂35%(碳酸氢钠与柠檬酸的配比为1∶2、黏合剂PVP 2%、润滑剂PEG4000 2%、矫味剂三氯蔗糖3%,余量为乳糖,制备过程中无黏冲现象,所得产品片崩解迅速,硬度符合要求。
按本研究最优工艺制得的泡腾片直径约为8 mm,重约为200 mg,硬度为5.5~6.5 kg,崩解时间<40 s,双平面圆形,表面光滑、整洁,遇水产生大量气体,崩解迅速。根据《中国药典》2015年版检测方法,对糖胺聚糖泡腾片的感官、重量差异、pH值、崩解时限、重金属和微生物限度等质量指标进行检测,试验结果如表12所示,均符合营养健康食品的相关要求[25]。
表12糖胺聚糖泡腾片质量指标检测结果
Tab.12Resultsofqualityindexofglycosaminoglycaneffervescenttablets

指标index结果result颜色colour白色外观surface双平面圆形,外形整洁,表面光滑口感风味taste口感柔和,微甜清爽,无杂质,具有特有的香气和滋味硬度hardness6.0 kg崩解时限disintegration time34 s质量差异weight difference(201.0±2.5) mg理化指标physicochemical index水分0.38%,蛋白质1.69%,总糖28.46%功能因子含量functional component合浦珠母贝糖胺聚糖50 mg污染物限量heavy metal limit铅≤0.06 mg/kg,总砷≤0.05 mg/kg,总汞≤0.05 mg/kg,镉≤0.06 mg/kg微生物限量microbial limit菌落总数<500 个/mL,霉菌<5 个/mL,酵母菌<50 个/mL,大肠杆菌、金黄色葡萄球菌、沙门氏菌未检出
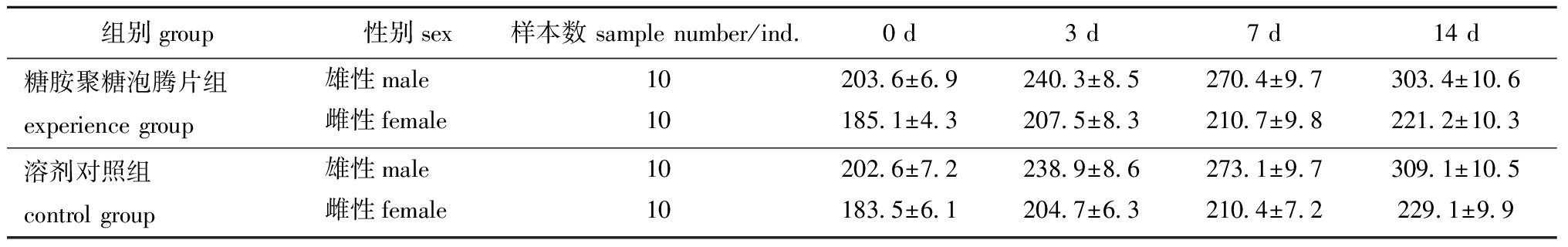
急性经口毒性试验主要是测定受试物的半数致死量或浓度,将试验动物1次或24 h内多次染毒,观察其中毒表现。试验结果显示,无论是在给予受试物过程中或14 d观察期内,合浦珠母贝糖胺聚糖泡腾片组和溶剂对照组中的雌、雄SD大鼠均无死亡,大鼠表现行为、呼吸、活动状况、姿势等均未见异常。将大鼠解剖后,肉眼观察其心脏、肝脏、脾、胃、生殖腺等脏器的外形、颜色、大小与比例,均未见任何异常。如表13所示,大鼠体质量正常增长,在各测定时间点,合浦珠母贝糖胺聚糖泡腾片组的大鼠体质量与溶剂对照组比较均无显著性差异(P>0.05)。因此,在本试验条件下,合浦珠母贝糖胺聚糖泡腾片对SD大鼠经口最大耐受剂量(MTD)高于15 g/kg,毒性分级为无毒。
表13SD大鼠急性经口毒性试验体质量结果
Tab.13BodyweightofSDratsintheacuteoraltoxicityexperimentsg
组别group性别sex样本数 sample number/ind.0 d3 d7 d14 d糖胺聚糖泡腾片组experience group雄性male10203.6±6.9240.3±8.5270.4±9.7303.4±10.6雌性female10185.1±4.3207.5±8.3210.7±9.8221.2±10.3溶剂对照组control group雄性male10202.6±7.2238.9±8.6273.1±9.7309.1±10.5雌性female10183.5±6.1204.7±6.3210.4±7.2229.1±9.9
泡腾片崩解剂由酸源和碳源共同组成,采用酸碱混合非水造粒法进行合浦珠母贝糖胺聚糖泡腾片的制备,可避免因崩解剂分开制粒产生的操作工序复杂、生产周期长等缺陷。本研究中选用PVP无水乙醇溶液作黏合剂,酸源和碳源可以同时制粒,此法不仅操作简单,而且酸碱接触充分,崩解时限短,但需要严格控制相对湿度和水分的引入[26]。本试验中经筛选,确定柠檬酸为崩解剂的酸源,郭冬艳等[27]在制备海棠泡腾片时也指出,柠檬酸作为酸源制成的泡腾片,其溶液具有澄明度高和口感好的特点。另外,崩解剂配比也是影响泡腾片品质的另一重要因素,张真真等[28]制备果皮提取物泡腾片的试验结果表明,碳酸钠与柠檬酸总量一定时,其配比为1∶1.6时压片效果最好,这与本试验结果1∶2略有差异,可能是因为其泡腾片中柠檬酸和碳酸钠总量比本试验的高,但宫江宁等[29]制备的紫苏提取物泡腾片中碳酸氢钠与柠檬酸的质量比为1∶2,与本试验结果相符。曹光环等[30]运用正交试验以崩解时限为指标,对崩解剂用量32%、37%、42% 3个水平进行优化,得到最优添加量为37%,而本试验得到的崩解剂添加量为35%,这从侧面印证了数据的可靠性。此外,片剂的崩解效果还受到片剂硬度的影响,随着片剂硬度增加,崩解时限延长,当控制片剂的硬度为5.0~7.0 kg时,片剂不易掉渣,崩解时限较短。
本研究中通过正交试验结果分析得到泡腾片最优配方为糖胺聚糖添加量25%,碳酸氢钠和柠檬酸总添加量35%(碳酸氢钠和柠檬酸比例为1∶2),PVP、PEG4000和三氯蔗糖添加量分别为泡腾片总质量的2%、2%、3%,余量为乳糖。按最佳配方制备的泡腾片色泽均匀,硬度适中,崩解时限短,根据《中国药典》2015年版检测方法,对糖胺聚糖泡腾片的感官、重量差异、硬度、崩解时限、重金属污染物和微生物限度等质量指标进行检测,均符合国家标准的相关要求。通过构建急性经口毒性大鼠模型,观察试验动物的中毒表现,证实其安全性较高。
参考文献:
[1] 申屠超,程青青,单伟光,等.金银花泡腾饮料片加工工艺的研究[J].食品工业科技,2012,33(12):255-258.
[2] 郑丽梅,潘宇,屈海涛,等.维生素C泡腾片制备工艺研究[J].黑龙江医药,2008,21(3):60-62.
[3] 范宝庆.黑莓泡腾片的研制[J].现代食品科技,2008,24(8):822-824.
[4] 邹柯姝,张殿昌,郭华阳,等.4种壳色合浦珠母贝贝壳棱柱层和珍珠质层7种金属元素质量分数的比较分析[J].南方水产科学,2015(3):74-79.
[5] 王琦,何毛贤.合浦珠母贝实时定量PCR内参基因的稳定性比较[J].南方水产科学,2013,9(6):33-40.
[6] 龙敏明,黄桂菊,邹记兴,等.育珠对合浦珠母贝N19和Prismalin-14基因表达水平的影响[J].南方水产科学,2013,9(5):58-63.
[7] 胡雪琼,吴红棉,范秀萍,等.近江牡蛎糖胺聚糖的免疫调节活性研究[J].现代食品科技,2014,30(12):16-24.
[8] 吴红棉,金晓石,范秀萍,等.珠母贝糖胺聚糖PG-Ⅱ诱导人宫颈癌HeLa细胞凋亡的研究[J].食品科学,2012,33(3):238-242.
[9] 胡雪琼,吴红棉,范秀萍,等.珠母贝糖胺聚糖抗肿瘤作用初步研究[J].食品工业科技,2013,34(22):315-319.
[10] 李孟婕.翡翠贻贝糖胺聚糖降血脂作用的研究[D].湛江:广东海洋大学,2011.
[11] 董晓静.波纹巴非蛤糖胺聚糖抗氧化与降血脂活性研究[D].湛江:广东海洋大学,2010.
[12] 周小双,王锦旭,杨贤庆,等.海洋动物糖胺聚糖的研究进展[J].食品安全质量检测学报,2015,6(12):4865-4870.
[13] 范嗣刚,王婧璇,黄桂菊,等.合浦珠母贝选育家系的遗传多样性分析[J].南方水产科学,2016,12(5):90-96.
[14] 周小双,王锦旭,杨贤庆,等.响应面法优化合浦珠母贝糖胺聚糖提取工艺[J].食品与发酵工业,2016,42(1):238-243.
[15] 郭栋,李红云.布洛芬分散片的处方筛选及制备[J].首都医药,2011(8):55-56.
[16] 李洋,罗玉琴,热依木古丽·阿布都拉,等.石榴皮提取物阴道泡腾片成型工艺的研究[J].中成药,2011,33(2):253-255.
[17] 张宏康,林奕楠,李德荣,等.番石榴泡腾片固体饮料研制[J].食品工业,2015,36(1):4-7.
[18] 孔妍.复方PBACC泡腾片的研制[D].天津:天津大学,2009.
[19] 中华人民共和国国家卫生和计划生育委员会.GB/T 15193.3—2014 食品安全国家标准 急性经口毒性试验[S].北京:中国标准出版社,2015.
[20] 郑丹丹,王京龙,张立华,等.竹叶提取物泡腾片的制备工艺优化及其质量分析[J].食品科学,2016,37(8):39-44.
[21] 杨春梅,吴金鸿,夏云,等.紫苏泡腾片固体饮料的研究[J].食品与药品,2012,14(11):381-385.
[22] 王宁,陈雪峰,王锐平.茶饮料泡腾片的加工工艺[J].食品与发酵工业,2007,33(3):151-153.
[23] 朱艳丽.盐酸甜菜碱泡腾片制备及部分药理作用研究[D].泰安:泰山医学院,2014.
[24] 周小双.合浦珠母贝糖胺聚糖的分离纯化、结构表征及免疫调节作用研究[D].上海:上海海洋大学,2016.
[25] 中华人民共和国国家卫生和计划生育委员会.GB/T 16740—2014 食品安全国家标准 保健食品[S].北京:中国标准出版社,2015.
[26] 于琛.绿茶维生素C泡腾片的研制[J].海峡药学,2012,24(11):27-29.
[27] 郭东艳,李瑾,董凯,等.多指标加权评分法优选海棠泡腾片的制备工艺[J].中成药,2011,33(9):1617-1620.
[28] 张真真,冯郑珂,林敏,等.常山胡柚果皮果渣提取物泡腾片制备工艺研究[J].安徽农业科学,2014(29):10291-10293,10325.
[29] 宫江宁,吴金鸿,王正武,等.紫苏提取物泡腾片的研制[J].食品科学,2013,34(6):280-284.
[30] 曹光环,张孝法,荣根新,等.橘红痰咳泡腾片制备工艺的研究[J].现代中药研究与实践,2010,24(1):43-45.
ZHANG Lei1, 2, WANG Jin-xu1, YANG Xian-qing1, WEI Ya1, YANG Shao-ling1
(1. Key Laboratory of Aquatic Product Processing, Ministry of Agriculture, National Research & Development Center for Aquatic Product Processing, South China Sea Fisheries Research Institute, Chinese Academy of Fishery Sciences, Guangzhou 510300, China; 2.College of Food Science and Technology, Shanghai Ocean University, Shanghai 201306, China)
Abstract:The preparation process and optimal formula of effervescent tablets with glycosaminoglycans extracted from pear oysterPinctadamartensiiwere investigated for enriching food variety and promoting high value utilization of shellfish. The effervescent tablets were prepared with glycosaminoglycan as the main material, and adhesives, lubricants, flavors and diluents as auxiliary materials by mixing raw materials, preparing granules, drying, and compression, and the formula was optimized by research of effects of the components on quality of the effervescent tablets in single factor experiments and orthogonal tests. The optimal formula (mass percentage) was comprised of 25% of glycosaminoglycans from the pearl oyster, mass ratio of sodium bicarbonate to citric acid=1∶2 at a dose of 35%, 3% of sucralose, 2% of PVP, 2% of PEG4000, and some lactose. The effervescent tablets are characterized by good taste and smooth surface by stable, reliable and easy accessible process, safety and nontoxicity by quality index detection and acute oral toxicity tests.
Keywords:Pinctadamartensii; glycosaminoglycan; effervescent tablet; orthogonal experiment; quality analysis
通信作者:杨贤庆(1963—), 男, 研究员。E-mail:yxqgd@163.com
作者简介:张磊(1993—), 女, 硕士研究生。E-mail:zhangleicx@163.com
基金项目:广东省自然科学基金资助项目(2016A030313144);广东省公益研究与能力建设专项 (2014A020217009);广东省渔港建设和渔业发展专项海洋渔业科技推广方向珍珠类项目(B201601Z05,B201601Z07); 广东省海洋渔业科技与产业发展专项科技攻关与研发项目(A201501C08)
收稿日期:2017-12-13
文章编号:2095-1388(2018)05-0644-07
DOI:10.16535/j.cnki.dlhyxb.2018.05.016
文献标志码:A
中图分类号:TS254.4